在再生醫學迅猛發展的今天,我們正見證著醫療理念從“控制癥狀”走向“修復神經”的革命性轉變。
在這一變革浪潮中,干細胞療法正在為許多長期依賴藥物控制、卻難以逆轉病程的神經退行性疾病帶來新的希望,其中,帕金森病的治療領域尤為引人關注。
然而,對于許多患者和家屬而言,“干細胞治療帕金森病” 仍然是一個既令人期待又略顯陌生的概念——為什么這些看似普通的細胞,能夠替代已經死亡的神經元?它們進入大腦后究竟如何發揮作用?與傳統藥物或腦深部電刺激相比,這種新療法到底帶來了怎樣的改變?
本文將帶您系統了解干細胞療法治療帕金森病的科學原理,解析它如何修復神經系統并改善帕金森病癥狀的,并結合臨床研究進展與未來方向,全面呈現這一前沿治療的真實圖景。

?一、帕金森病的核心困境:多巴胺神經元的凋零
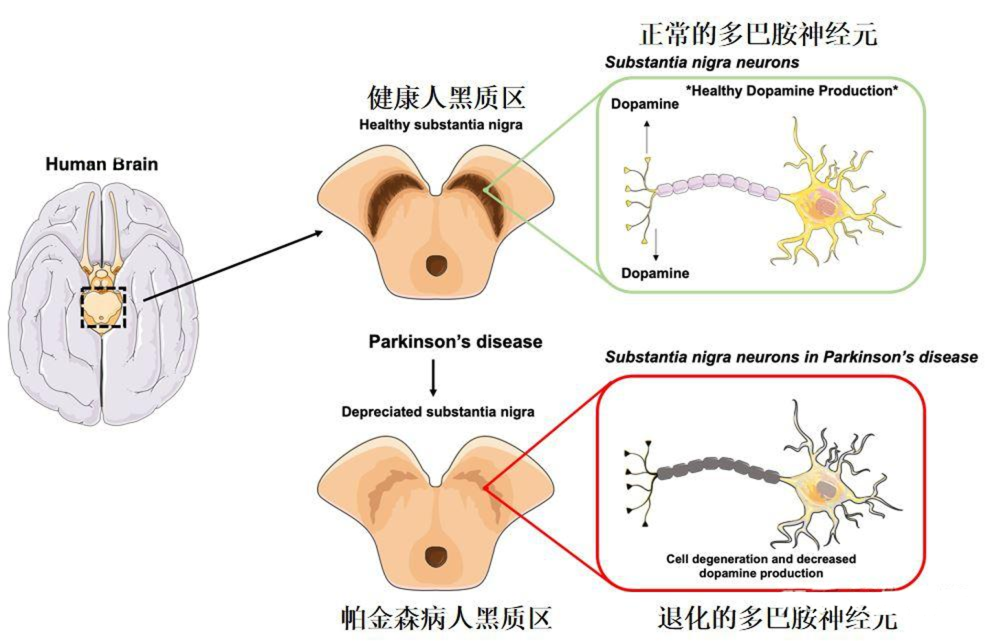
理解干細胞療法,必須從帕金森病的根源開始。該病的核心病理變化發生在中腦一個名為“黑質”的區域——這里分泌多巴胺的神經元發生進行性、不可逆的死亡。
多巴胺是大腦中關鍵的神經遞質,負責協調精細運動。當這些細胞喪失超過60-80%時,運動功能障礙便會顯現。
傳統藥物治療的局限性當前主流的左旋多巴等藥物,如同為枯竭的泉水臨時引水,只能補充多巴胺,卻無法阻止神經元的繼續死亡。
隨時間推移,藥物療效逐漸減退,還會引發劑末現象、異動癥等副作用。全球近1000萬帕金森病患者中,約40%在治療5年后出現嚴重并發癥。
二、什么是干細胞療法?它與傳統治療的根本區別
干細胞療法代表了一種全新的治療范式,其核心理念與傳統方法有根本性區別。我們可以用一個簡單比喻來理解:
- 傳統藥物治療(如左旋多巴):如同給干涸的土地持續澆水——暫時補充缺失的多巴胺,但無法阻止水源(神經元)的持續流失。隨著病程發展,需要的水量越來越大,效果卻越來越差,還可能引發”劑末現象”和”異動癥”等并發癥。
- 干細胞療法:則像是直接播種新的水源。它不再滿足于臨時補充,而是致力于從根本上修復生態系統——替換那些已經死亡的多巴胺能神經元,重建大腦正常的神經調節網絡。
核心機制:利用干細胞這種具有自我更新和定向分化能力的”萬能種子”,在實驗室精心培養和誘導后,通過精準的神經外科手術移植到患者大腦的特定區域。這些細胞將在腦內成熟為功能性的多巴胺神經元,與現有神經網絡建立連接,從源頭上恢復多巴胺的自主分泌和運動功能的持久調節。
這種從”替代治療”到”再生修復”的轉變,正是干細胞療法最具革命性的突破——它不僅控制癥狀,更直指疾病根源,為帕金森病的長期管理提供了全新的可能性。
三、?干細胞療法是如何起作用的?
干細胞移植后通過三重協同機制發揮治療作用,形成全方位的修復網絡:
1. 直接細胞替代:移植的干細胞在腦內分化為成熟的多巴胺能神經元,直接填補因疾病喪失的細胞空缺。這些”新生代神經元”能夠整合到現有神經回路中,自主分泌多巴胺,恢復運動調節功能。
2. 神經營養支持:干細胞持續分泌腦源性神經營養因子、膠質細胞源性神經營養因子等多種營養因子,為殘存的神經元提供保護,延緩其退化進程,創造有利于神經修復的微環境。
3. 免疫調節與抗炎:研究證實,干細胞能夠調節腦內過度活躍的免疫反應,減輕慢性神經炎癥——這是導致神經元進行性死亡的關鍵因素之一。通過抑制有害的免疫反應,干細胞為神經修復創造有利條件。
這三重機制相互協同,共同構建了一個自我維持的修復系統,為帕金森病的長期改善提供了可能。
四、治療帕金森病的常用干細胞類型:各有特點與優勢
目前用于帕金森病研究的干細胞主要分為四類,各有其取材來源、安全性和應用潛力:?
| 干細胞類型? | 來源? | 核心優勢? | 應用現狀? |
| 神經干細胞? | 胎兒腦組織、誘導分化? | 可直接分化為多巴胺能神經元,與帕金森病所需修復的損傷部位高度匹配,神經特異性高? | 近年研究熱點,多項研究顯示可改善運動癥狀與腦功能指標 |
| 間充質干細胞? | 骨髓、臍帶、脂肪組織? | 取材便捷、免疫原性極低(不易引發排斥)、可批量獲取? | 臨床研究最廣泛,安全性已初步驗證? |
| 誘導多能干細胞 | 患者自體體細胞(如皮膚細胞)重編程? | 可 “個性化定制”(避免免疫排斥)、可定向分化為高純度多巴胺能神經元? | 近年研究熱點,部分進入早期臨床試驗? |
| 胚胎干細胞? | 早期胚胎? | 分化能力最強,可生成各類神經細胞? | 倫理爭議大,多數國家限制臨床應用? |
其中,神經干細胞以及誘導多能干細胞因其高度針對性和更接近疾病本質的修復機制,正成為研究與臨床探索的重點方向。
五、臨床研究進展:從實驗室走向患者的 “關鍵突破”
近年來,干細胞療法治療帕金森病的臨床研究已從 “基礎實驗” 逐步邁向 “人體試驗”,多項臨床試驗結果顯示出積極潛力:
國內首例自體iPSC神經細胞移植,實現從“患者”到“見證者”的突破
在第29個世界帕金森病日來臨前夕,中國首例帕金森病患者接受GCP級自體干細胞移植治療的帕金森病患者,2025年4月8日現身上海瑞金醫院科普活動現場,首度面向公眾分享其階段性康復體驗。[1]
這也意味著,中國首例帕金森病患者通過國際標準臨床試驗,用自身干細胞修復受損腦神經,邁出細胞治療帕金森病的關鍵一步。

作為我國首位通過國家藥監局批準的GCP級臨床試驗參與者,沈女士于3月1日接受手術,通過微創方式將自體誘導多能干細胞(iPSC)分化的多巴胺能神經前體細胞移植至腦內特定區域。
術后僅1個月,她已實現全天自主行走,睡眠質量顯著改善,肢體僵硬與震顫癥狀明顯緩解。這一案例標志著我國在 細胞治療帕金森病領域 取得重大突破,為全球神經退行性疾病治療提供了“中國方案”。
沈女士在分享中提到:
“手術后第二天就能下地走路,睡眠質量從每晚2小時提升到6小時”;
“每天都能感受到細微進步,這種‘向好’的感覺讓我重拾信心”;
“希望未來更多患者能像我一樣,不必終生效藥物控制”。
這一案例標志著我國在細胞治療帕金森病領域邁出了關鍵一步,為全球神經退行性疾病的創新治療提供了全新的“中國方案”。
亞洲首次人胚胎干細胞神經元移植試驗,驗證安全性與有效性的新里程碑
2025年10月14日,延世大學Severance研究團隊公布了亞洲地區首次、全球范圍內第二次報道的通過移植源自人胚胎干細胞的A9型多巴胺前體細胞(A9-DPC),成功實現了對中重度帕金森病患者的精準治療。[2]

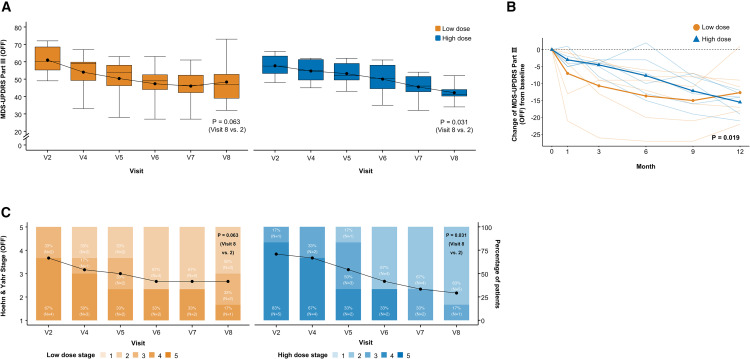
這項單中心、開放標簽的臨床試驗歷時12個月,納入12名病程超過5年的帕金森病患者。通過立體定向手術,將細胞精確移植至患者雙側殼核區域,其中低劑量組(315萬細胞)和高劑量組(630萬細胞)各6例。
研究數據顯示,干細胞移植在安全性方面表現良好。整個試驗中僅出現少量輕微不良反應,多與免疫抑制藥物相關,無嚴重并發癥或細胞異常增殖。影像學結果也證實,移植細胞精準分布,無異常遷移或腫瘤形成。
療效方面,患者在術后12個月運動功能平均提升14分以上,高劑量組效果更為顯著。日常活動能力、生活質量及藥效持續時間均有明顯改善。分子影像學進一步驗證了這一變化:移植區域的多巴胺轉運體活性顯著增強,說明移植細胞成功整合進神經系統,部分恢復了多巴胺通路功能。
組織分析顯示,移植的細胞已在宿主體內分化為成熟的多巴胺神經元,并與原有神經網絡形成有效連接。這一結果標志著人源胚胎干細胞衍生細胞治療帕金森病的安全性與可行性得到初步驗證,為未來大規模臨床應用奠定了基礎。
該研究的最大突破,在于首次系統驗證了人胚胎干細胞衍生神經元治療帕金森病的可行性與安全性。與過去依賴胎兒組織移植不同,這一方案在倫理、來源及生產標準上都實現了突破。采用新鮮細胞移植的策略,也最大限度地保留了細胞活性。科學的劑量設計,源自前期動物實驗的積累,使得療效更具可靠性。
詳情請瀏覽:2025干細胞療法治療帕金森病最新臨床指南(截至10月)
六、現存挑戰與未來方向:讓 “希望” 落地的關鍵
盡管干細胞療法為帕金森病治療帶來了革命性希望,但從實驗室成果轉化為穩定、可靠的臨床方案,仍有一段關鍵路程需要跨越。當前面臨的核心挑戰主要集中在以下幾點:
首先,移植細胞的存活與整合效率仍需提升。研究表明,移植后僅有部分細胞(約15-30%)能在復雜的大腦環境中長期存活并成功融入原有的神經回路,發揮功能。這好比將珍貴的種子播撒后,需要確保它們能在新“土壤”中扎根生長。
其次,治療的標準化與安全性需持續驗證。如何精確控制細胞分化、確保無腫瘤風險、并最小化免疫排斥,是大規模臨床應用前必須解答的問題。
針對這些挑戰,未來的突破方向正變得清晰:
- 活體監測技術:運用先進的影像學手段,實時追蹤移植細胞在體內的命運,實現療效的可視化評估。
- 基因工程技術:通過編輯干細胞基因,增強其抗凋亡和適應能力,讓移植細胞更“頑強”。
- 新型生物材料:開發仿生支架或凝膠,為移植細胞提供支撐與營養,創造一個更友好的生存微環境。
- 個體化精準醫療:結合患者基因圖譜與疾病特征,定制專屬的細胞療法方案。
結語:不止于“緩解”,更向“治愈”靠近
帕金森病的治療正在經歷從“對癥”到“對因”的歷史性轉變。干細胞療法代表著這一轉變的最前沿——它不僅旨在緩解顫抖,更致力于修復顫抖的根源。
全球超過200項相關臨床試驗正在進行,每項研究都在為最終的安全有效治療積累寶貴數據。雖然前路仍有科學難題需要攻克,但每一次移植嘗試,都為千萬帕金森病患者帶來重獲生活品質的新希望。
科學的價值在于將不可能變為可能。隨著再生醫學、基因工程和神經科學的深度融合,根治帕金森病這一愿景,正從遙不可及的未來,逐漸變為可規劃的現實路徑。
對于正在與疾病抗爭的患者而言,了解這些進展不僅是獲取信息,更是儲備希望——在醫學不斷突破邊界的時代,今天的尖端研究,可能就是明天的常規治療。
參考資料:
[1]https://mp.weixin.qq.com/s/FvDBPHYykFR83WXTdBH-VA
[2]Phase 1/2a clinical trial of hESC-derived dopamine progenitors in Parkinson’s diseaseChang, Jin Woo et al.Cell, Volume 0, Issue 0
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信