帕金森病(PD)作為第二常見的神經退行性疾病,其病理核心是中腦黑質多巴胺能神經元的進行性喪失。現有療法僅能緩解癥狀,無法逆轉疾病進程。干細胞療法,特別是誘導多能干細胞(iPSC)技術的興起,為帕金森病的根本性治療帶來了新希望。本文系統綜述了iPSC療法在帕金森病治療中的最新進展、關鍵方法、臨床轉化挑戰以及未來發展方向。
引言:神經退行性疾病,如帕金森病(PD),以中樞神經系統神經元逐漸退化為特征,最終導致腦功能進行性受損。干細胞療法,包括胎兒中腦細胞、人類胚胎干細胞(hESCs)及人類誘導多能干細胞(hiPSCs),為神經修復提供了潛在途徑。其中,hiPSCs因其可來源于患者體細胞、規避倫理爭議并降低免疫排斥風險,成為再生醫學的研究熱點。

《神經科學》雜志揭秘:iPSC療法治療帕金森病的療效與挑戰
2026年1月24日,《神經科學》雜志發表了一篇聚焦于“誘導多能干細胞療法在帕金森病治療中的療效、方法與挑戰”的綜述文章。本文在此基礎上,進一步梳理該領域的關鍵進展,探討hiPSCs在帕金森病治療中的轉化潛力與現存瓶頸[1]。
帕金森病的疾病本質、病理特征與流行病學
帕金森病是一種進行性神經退行性疾病,其核心病理變化位于中腦的黑質致密部,表現為該區域負責產生多巴胺的神經元不可逆地、漸進性死亡。這一神經元丟失的直接微觀證據是腦內出現稱為“路易體”的異常蛋白質聚集體,其主要成分是錯誤折疊的α-突觸核蛋白。

從全球范圍看,該病是僅次于阿爾茨海默病的第二大常見神經退行性疾病,流行病學數據顯示其年齡標準化發病率大約在每10萬人年8至18例之間,表明其是一個重要的公共衛生問題。
臨床表現與當前治療困境:帕金森病的癥狀復雜多樣,主要分為運動與非運動兩大類。經典的運動癥狀包括靜止性震顫、動作遲緩、肌強直和姿勢步態異常,這些癥狀直接與腦內多巴胺缺乏相關。此外,患者普遍遭受一系列非運動癥狀的困擾,如嗅覺失靈、情緒認知障礙、睡眠紊亂等,這些癥狀往往更早出現且嚴重影響生活質量。
盡管現代醫學通過藥物(如左旋多巴)和手術(如深部腦刺激)手段能夠有效控制部分運動癥狀,但所有現有療法均屬于對癥治療,無法從根本上延緩或阻止黑質多巴胺能神經元的退化進程,這構成了當前臨床治療的主要局限(圖1)。
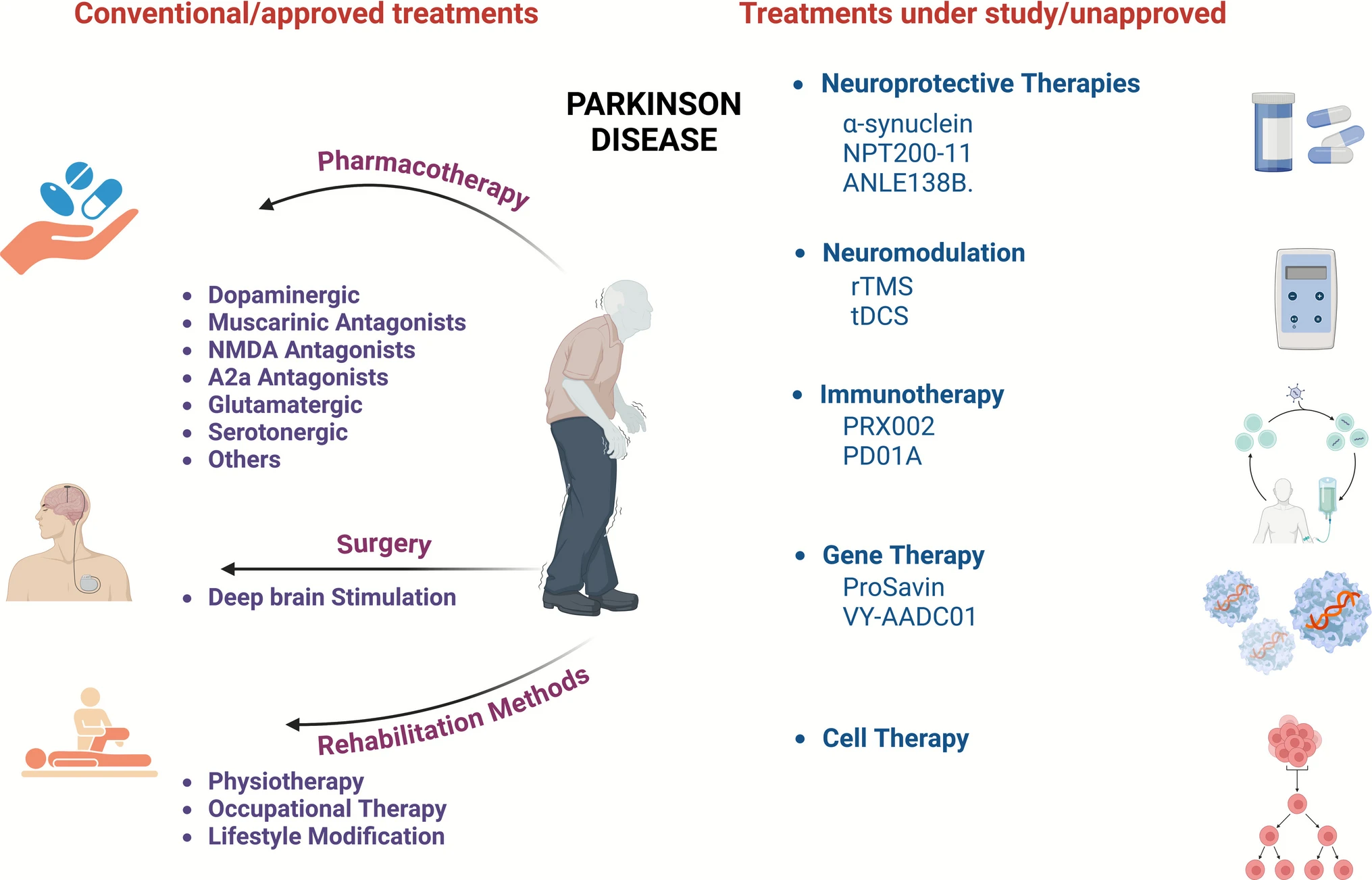
發病機制與干細胞治療的潛力:帕金森病的病因是多因素交互作用的復雜結果,涉及遺傳易感性、環境毒素暴露、細胞自噬功能失調、慢性神經炎癥以及衰老本身。這些因素共同導致了最終的神經元變性。為突破傳統療法無法修復神經元的瓶頸,研究人員將目光投向以細胞替代為目標的再生醫學。
其中,干細胞移植(特別是神經干細胞和誘導多能干細胞)展現出巨大潛力。這些細胞具有強大的自我更新和多向分化能力,能夠在特定條件下被誘導分化為多巴胺能神經元,理論上可直接補充丟失的細胞。尤其是利用患者體細胞重編程獲得的誘導多能干細胞,不僅解決了胚胎干細胞的倫理爭議,通過非整合重編程技術(如使用質粒、RNA等)也避免了基因組改變的安全風險,為個體化、根源性的治療帶來了新希望。
什么是帕金森病的細胞療法?
帕金森病細胞療法是一種旨在通過移植新的、功能正常的多巴胺能神經前體細胞(或祖細胞),替代患者大腦中已經退化的同類神經元,以重建受損的神經回路并持久緩解癥狀 的再生醫學方法。其核心原理與操作要點可概括如下:
治療原理與靶點:帕金森病(PD)的病理特征是位于中腦黑質區域的多巴胺能神經元發生退化(圖2)。這些位于中腦的多巴胺(DA)神經元投射神經突至殼核和尾狀核,并在這些區域釋放多巴胺作為神經遞質,在帕金森病中發生退化。因此,殼核內的多巴胺水平降低。細胞療法直接針對這一根本缺陷,通過補充能產生多巴胺的細胞來恢復神經化學平衡。
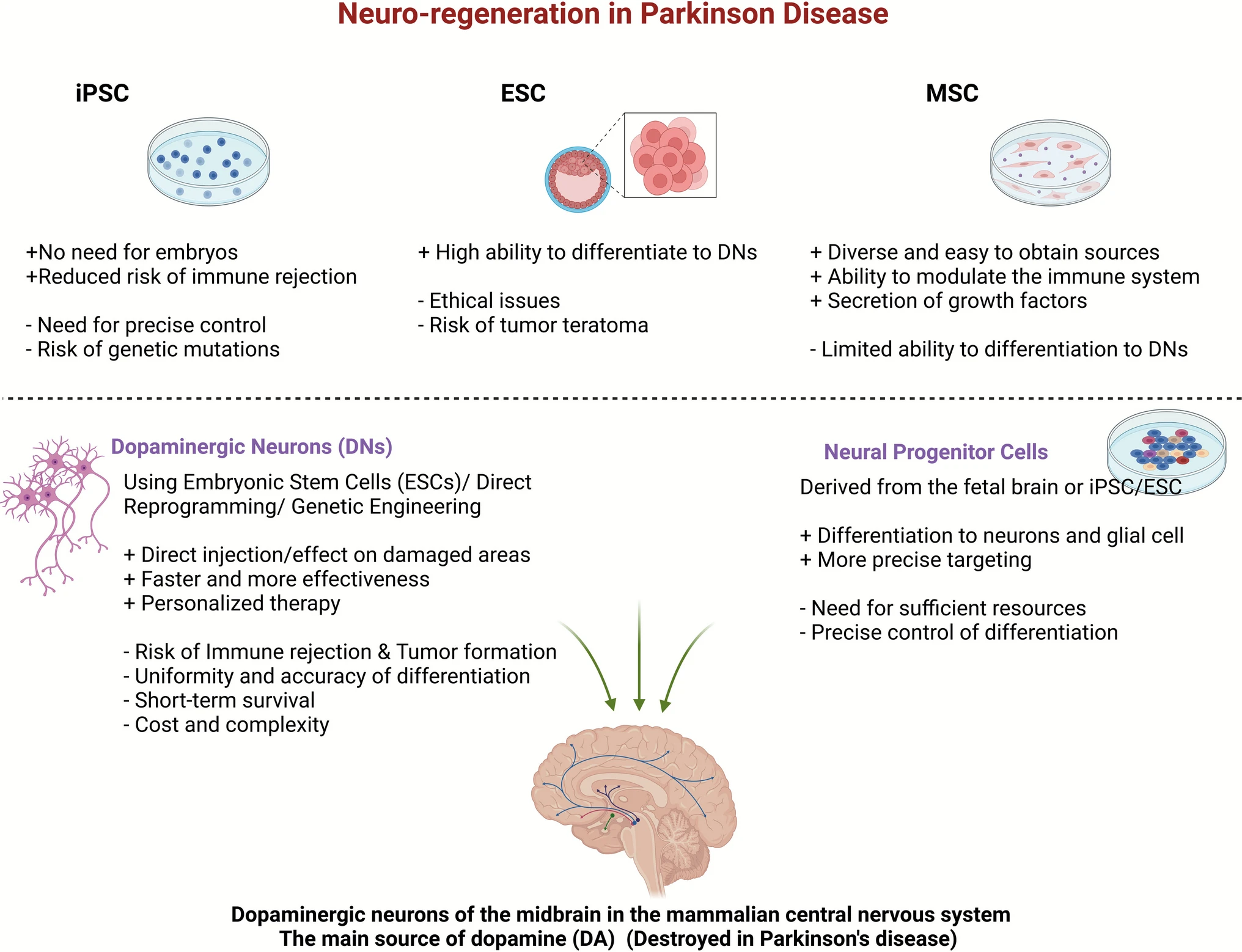
操作方法:目前主流的方法是異位移植,即將在實驗室中培養、處于未成熟發育階段的多巴胺能神經祖細胞,直接注射到癥狀相關的腦區——殼核內。移植細胞能在該部位存活、分化為成熟神經元,并長出神經突起,與宿主腦細胞建立功能性突觸連接,從而“橋接”并修復受損的多巴胺信號通路。盡管也有研究嘗試將細胞移植回其原生位置黑質(同位移植),但證據顯示這種方法帶來的功能改善不如移植到殼核顯著。
療效與證據基礎:該療法的臨床經驗主要來源于歷史上移植人類流產胎兒黑質組織的研究。數據顯示,移植成功后,患者的功能改善通常在移植后數月才開始顯現,并可能持續恢復超過4年,之后進入一個較長的病情穩定平臺期。這表明成功的細胞移植能夠實現長期的生物學整合,并提供持久療效。
總結而言,帕金森病細胞療法是一種從疾病根源入手、修復性而非單純對癥的治療策略。它利用移植的細胞作為“活體藥物”在大腦內定植、整合并發揮功能,以期實現癥狀的長期緩解與病情進展的阻滯。
基于iPSC的帕金森病治療:從研究到臨床
一、歷年研究進展:從實驗室到臨床
iPSC治療帕金森病的研究已取得實質性突破,正從概念驗證走向臨床早期應用。
臨床前研究深化:2025年發表于《細胞-干細胞》的一項研究,在嚴格規范下驗證了利用帕金森病患者自身細胞制備iPSC并分化為多巴胺能細胞的安全性和可行性,為開展自體治療臨床試驗奠定了基礎。

國際臨床試驗驗證安全性:2025年《自然》期刊同期發表了兩項早期臨床試驗結果。日本的試驗顯示,7名患者接受iPSC來源的細胞移植后,在24個月內未出現嚴重副作用或腫瘤。這初步證明了該療法在人體中的安全性。

中國取得突破性臨床結果:2025年10月,中國報道了全球首例早發型帕金森病患者在接受iPSC衍生細胞(“NCR201”注射液)移植后3個月實現“功能性治愈”的案例。患者運動功能、生活質量和腦內多巴胺活性影像學指標均得到顯著恢復。此前在2025年4月,中國也完成了首例自體iPSC治療帕金森病患者的移植手術。
二、技術優化方向:追求純度、安全與穩定
為推進臨床應用,當前的研究重點聚焦于以下幾個核心優化方向:
分化方案的優化:目標是獲得高純度、特定功能亞型(如中腦黑質致密部的A9型)的多巴胺能神經元。中國的研究團隊已報道了能分化出高純度A9神經元的方法。三維腦類器官等新模型也在探索中,以更真實地模擬大腦環境。
安全性與質控體系的建立:這是臨床轉化的關鍵。優化重點包括:采用非整合重編程技術(如附加體型載體)避免基因突變風險;建立嚴格的細胞產品釋放標準,對基因組完整性、致瘤性等進行全面檢測;開發清除未完全分化iPSC的方法,從源頭降低腫瘤風險。
解決個體差異與標準化生產:研究發現,不同患者來源的iPSC分化出的細胞,其治療效果可能存在差異。這推動了對穩定、可預測的細胞產品的需求。通用型(異體)iPSC產品通過建立與人群HLA配型的“細胞庫”,有望實現標準化、規模化生產,降低成本。
三、中國開展的臨床試驗:自體與通用型路徑并行
目前,中國在該領域的臨床研究非常活躍,主要沿著兩條技術路徑推進:
自體iPSC療法:使用患者自身的細胞制備,理論上可避免免疫排斥。
- 代表項目是上海瑞金醫院與中科院團隊合作的“UX-DA001注射液”。首例66歲的患者已于2025年3月完成移植,術后早期即觀察到運動癥狀改善。
通用型(異體)iPSC療法:使用健康供者細胞建立干細胞庫,經過配型后使用,優勢是“現貨”供應。
- 代表產品是安徽中盛溯源的“NCR201注射液”。該產品已獲得國家藥監局臨床試驗批準,其針對早發型帕金森病患者的臨床研究取得了前述突破性結果。目前,由首都醫科大學宣武醫院牽頭的該產品臨床試驗正在公開招募受試者。

移植方法與免疫考量
細胞療法通常需要考慮患者免疫系統排斥移植細胞的風險。雖然過去認為大腦是免疫系統活性較低的區域,但這一觀點目前正在重新評估。既往胎兒細胞移植的臨床經驗表明,使用免疫抑制劑可以改善治療效果。基于干細胞的移植提供了多種解決免疫排斥問題的方法:
- 自體移植:使用患者自身的細胞。
- 非HLA配型的同種異體移植:供體和受體之間不進行HLA配型。
- HLA配型的同種異體移植:供體和受體之間進行HLA配型。
- 使用“通用型”多能干細胞。
“通用型”多能干細胞是指經過基因改造、以降低或消除HLA分子表達的多能干細胞。通過基因編輯抑制或消除HLA分子的表達,能使“通用型”多能干細胞避開宿主主要的HLA相關免疫反應。不過,對于這類細胞,也必須考慮到與自然殺傷(NK)細胞和次要抗原相關的潛在免疫反應。已有數種策略被報道,旨在將NK細胞對“通用型”多能干細胞的反應降至最低。
總體而言,這些“通用”供體干細胞預計將達到臨床應用階段,因為從理論上講,它們最能防止與移植物相關的免疫反應。目前,針對帕金森病(PD)的基于多能干細胞干預措施的唯一臨床研究,要么采用了伴隨免疫抑制藥物的同種異體移植,要么采用了自體移植。
結論與展望
iPSC衍生神經元不僅為帕金森病的病理機制研究與藥物篩選提供了強大平臺,更展現出顯著的臨床治療潛力。盡管目前的研究成果令人鼓舞,但其向常規治療的轉化仍面臨諸多挑戰:包括細胞產品的安全性、純度與功能性標準化;個體療效差異的調控;以及長期移植后的免疫監控與功能評估。
未來,通過持續優化分化協議、完善質控體系、推進通用型細胞庫建設,并開展嚴謹設計的臨床試驗,iPSC療法有望為帕金森病患者帶來根本性、個體化的治療突破。我們謹慎樂觀地認為,在不久的未來,這些科學與技術障礙將被逐步克服,推動該療法真正走向臨床普及。
參考資料:
[1]:Mustafa, M.A., Al-Hasnaawei, S., Kaur, I. et al. Investigating the efficacy, methods, and challenges of induced pluripotent stem cells (iPSC) therapy in Parkinson’s disease. Neurol Sci 47, 190 (2026). https://doi.org/10.1007/s10072-025-08719-1
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信