近日,“人臍帶間充質干細胞(UC-MSC)治療2型糖尿病技術”在海南博鰲樂城國際醫療旅游先行區獲批進入臨床轉化應用階段。這標志著針對部分糖尿病人群的干預手段,正式從“實驗室研究”邁向“臨床可及”,也為糖友提供了一種全新的治療選擇。
同為干細胞治療糖尿病,5.8萬一次的糖尿病應用為何比1.98萬的“藥”更貴?

一、從“研究”到“應用”,意味著什么?
“臨床轉化應用”在醫學上是一個關鍵節點,它至少傳遞出兩層重要信息:
安全性獲得階段性認可:這意味著該技術已積累了一定的人體應用數據,在監管與倫理的雙重監督下,其安全性與耐受性已達到可繼續在臨床中驗證的水平。對于直接回輸人體的細胞治療而言,安全是首要前提。
療效顯現出臨床價值信號:相比早期的實驗室研究,進入轉化階段通常基于前期臨床觀察——在特定適應癥人群中,該技術已顯示出具有統計學意義的改善趨勢,值得進一步擴大應用以驗證其療效。

二、5.8萬/次vs1.98萬/支:差價從何而來?
不少讀者注意到,國內已上市的一款用于治療移植物抗宿主病(GvHD)的干細胞藥物,單支定價約1.98萬元,而此次糖尿病治療單次費用為5.8萬元。這背后的差異主要源于治療策略與階段的不同:
劑量與療程設計不同:GvHD治療通常需短期高頻輸注(如一療程8次),單次細胞量相對較低,總費用約15.8萬元。

糖尿病治療則側重于慢性修復,單次細胞輸注量較大(如5000萬單位),但頻次低(常見為3次一療程),總費用約17.4萬元,兩者總療程成本處于相近量級。
“上市藥品”與“特許技術”的區別:1.98萬元對應的是已獲批上市、可批量生產的標準化藥品;5.8萬元對應的是在先行區開展、按個體化制備與監護的臨床轉化技術,包含更精細的工藝、質檢與醫療管理成本。

三、臍帶間充質干細胞治療糖尿病的科學邏輯
UC-MSC受到關注,并非因為它是“神奇藥物”,而是基于其明確的生物學機制:
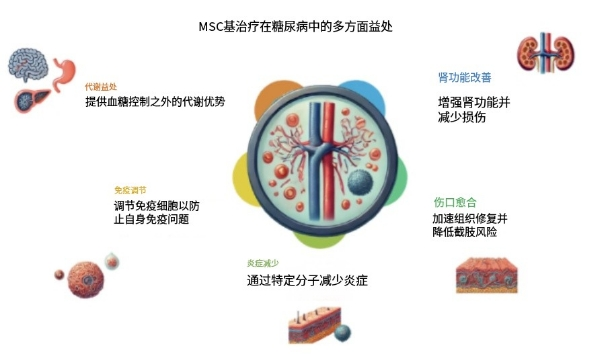
調節免疫,減輕炎癥:2型糖尿病常伴隨慢性低度炎癥,UC-MSC可通過調控免疫細胞、分泌抗炎因子,改善胰島局部微環境,為胰島β細胞修復創造條件。
改善胰島素抵抗:部分臨床研究提示,UC-MSC輸注后,患者外周組織對胰島素的敏感性有所提升,這有助于打破高血糖與胰島素抵抗之間的惡性循環。
四、哪些人可能適合?
臨床轉化有明確的適應癥范圍,當前主要面向以下兩類人群:
復雜難控型2型糖尿病患者:即在規范使用多種口服降糖藥及胰島素后,血糖仍持續不達標、波動大的患者。
尋求代謝功能改善與生活質量提升者:對于希望減少藥物依賴、延緩并發癥,且對前沿醫學技術有了解和接納意愿的人群,這提供了一個在標準治療之外的新選項。

五、如何看待“先行者成本”?
一項前沿生物醫療技術在早期應用階段,定價往往較高。17.4萬元/療程的背后,是細胞制備、質控、長期隨訪及嚴密醫療監護的綜合成本。
從醫學發展進程看,此類“先行先試”的價值在于時間差優勢——在全國普及、進入醫保之前,為符合條件的患者提供了一個提前選擇的窗口。這不僅關乎血糖數字的變化,更關乎治療邏輯從“控制癥狀”向“修復調節”的思維轉變。
結語
干細胞治療糖尿病,正逐漸從科研探索走向臨床現實。隨著轉化應用的推進,這種基于再生醫學的策略,有望填補傳統藥物與手術之間的治療空白,為部分糖友提供新的治療路徑。
當然,任何新技術都需理性看待:它并非根治手段,也非人人適用。患者應在專業醫師指導下,結合自身病情、經濟條件與治療預期,做出審慎選擇。
信息來源:干細胞與基因科學
聲明:本文僅供信息交流參考,不構成醫療建議。內容不代表任何機構立場,亦無商業推薦意圖。部分內容由AI輔助生成,并經人工審核整理。



 掃碼添加官方微信
掃碼添加官方微信