近幾年,從國家到地方,政策也愈加清晰地展示對發展生物科技,發展細胞治療技術的重視,也預示著我國干細胞行業在國家政策的支持下進入快速發展期。
接下來闡述我國干細胞的臨床應用研究的發展歷程和現狀:
01
我國干細胞臨床研究及應用的監管政策發展歷程
第一階段:起步期(1993-2003 年)期間發布的主要政策如下
1、1993年?—?原衛生部?《人的體細胞治療及基因治療臨床研究質控要點》
2、1999年 — 國家藥監局 《新生物制品審批辦法》
3、2003年 — 國家食藥監局 《人體細胞治療研究和制劑質量控制技術指導原則》
國家衛生主管部門和藥品監管部門陸續出臺細胞應用研究相關政策,意味著我國人的體細胞治療領域進入科學化、規范化、與國際同步的良好發展開端。

第二階段:成長期(2009-2015 年)期間發布的主要政策如下
1、2009年 原衛生部 《醫療技術臨床應用管理辦法》
2、2015年 原衛計委 《關于取消第三類醫療技術臨床應用準入審批有關工作的通知》
3、2015年 原衛計委聯合食藥監局 《干細胞臨床研究管理辦法(試行)》、《干細胞制劑質量控制及臨床前研究指導原則(試行)》
隨著細胞產業的發展,細胞應用研究相關政策不斷完善,在臨床研究方面,干細胞治療得以從人的體細胞治療中分類出來,得到明確的專門管理辦法,并適用至今。干細胞臨床研究開始施行備案管理制度,標志著干細胞行業發展迎來風口。
第三階段:快速發展期(2017-至今)期間發布的主要政策如下
1、2017年 國家食藥監局 《細胞治療產品研究與評價技術指導原則(試行)》
2、2018年 國務院 《關于支持自由貿易試驗區深化改革創新若干措施的通知》
3、2019年 國家衛健委聯合藥監局 《關于做好2019年干細胞臨床研究監督管理工作的通知》
4、2020年 國家藥監局藥審中心《人源性干細胞及其衍生細胞治療產品臨床試驗技術指導原則(征求意見稿)》
5、2021年 國家藥監局藥審中心《人源性干細胞產品藥學研究與評價技術指導原則(征求意見稿)》截至2021年12月31日,CDE共發布17個相關指南(試行和征求意見稿合并),最早可追溯至2008年發布的《人體細胞治療研究和制劑質量控制技術指導原則》和《人基因治療研究和制劑質量控制技術指導原則》。
國家政策進一步推動干細胞產業發展,衛健委備案干細胞臨床研究機構和項目逐年增多,國家藥監局啟動干細胞治療產品申報;各省市地方也做出積極響應,相繼發布多項利好政策,鼓勵干細胞治療行業規范化蓬勃發展。

02
我國干細胞臨床研究發展現狀
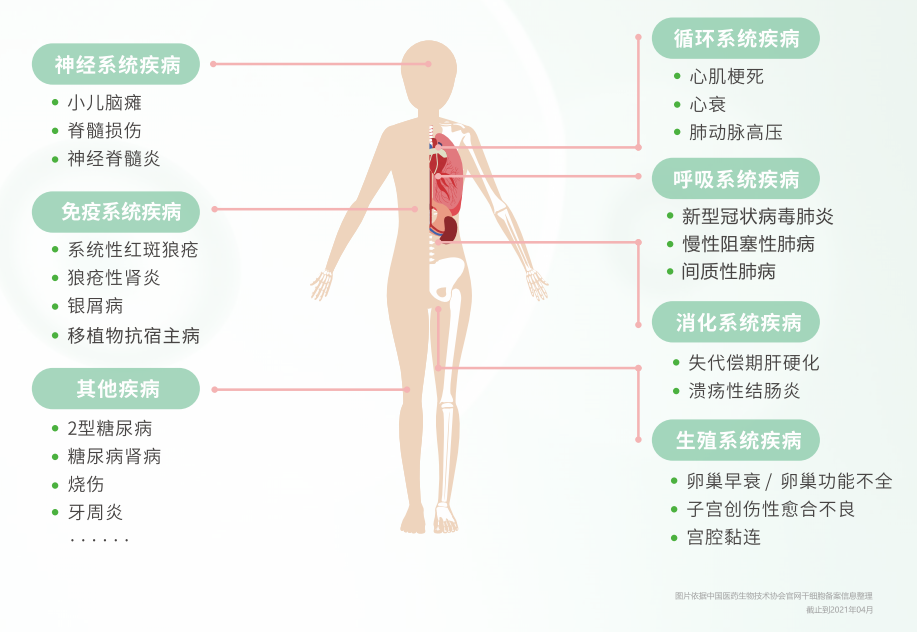
截止到2022年1月,全國已有111家研究機構(不含部隊醫院)、111個干細胞臨床研究項目通過國家衛健委成功備案。其中明確使用間充質干細胞占據了79項,項目占比達到了71.17%。以神經系統疾病、生殖系統疾病(卵巢早衰、子宮修復)及自身免疫疾病為主。
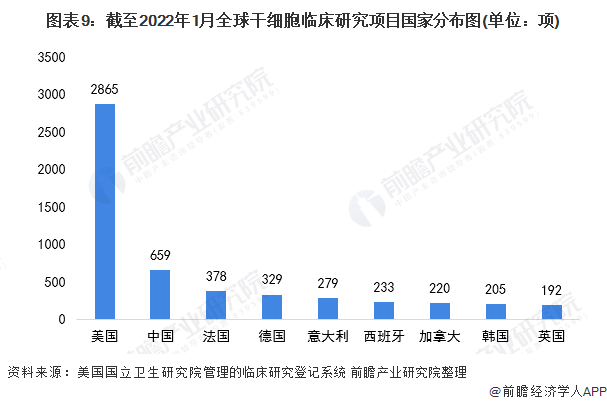
根據美國國立衛生研究院管理的臨床研究登記系統(Clinicaltrials.gov)數據顯示,截至2022年1月4日,全球登記的干細胞臨床研究項目共計6065項,涉及糖尿病、骨關節炎、卒中、帕金森和脊柱損傷、血液系統疾病、神經系統疾病、肢體缺血性疾病、心腦血管疾病、分泌系統疾病、外科疾病、皮膚病、腫瘤和免疫系統等上百種疾病。
其中美國保持絕對領先的地位,美國干細胞臨床研究項目數量達到2865項,中國、法國和德國的干細胞臨床研究項目數量分別為659項、378項和329項。截至2021年12月,全球已經有21款干細胞產品獲批上市,分布于美國、歐盟、韓國、加拿大、澳大利亞和日本等地。
根據國家藥品監督管理局藥品審評中心(CDE)公示信息顯示,截止2021年12月,共有19個干細胞新藥項目獲得國家臨床默示許可。分別是胎盤、臍帶、牙髓、宮血、異體/自體脂肪來源的間充質干細胞,適應證包括了膝骨關節炎、類風濕關節炎、糖尿病足潰瘍、銀屑病、肺纖維化、肝衰竭、卒中、急性呼吸窘迫綜合征、牙周炎、克羅恩病和 GvHD等。
03
政策支持干細胞臨床轉化,前景廣闊
在我國,預計到2050年,60歲以上老年人口將達到5億,類似的人口結構也正影響著全球各國,這些因素正在加速細胞治療領域的發展。傳統的藥物治療,雖然曾讓肺炎、梅毒、肺結核等過去的不治之癥成功被治愈,但對非感染導致的疾病(例如糖尿病、高血壓、心臟病等疾病)收效甚微。隨著細胞治療時代的到來,干細胞為疾病治療帶來了更有效的新方法,讓患者由內而外獲得新生。
干細胞產業在我國“十三五”規劃、“十四五”規劃和《“健康中國2030”規劃綱要》中,都是國家發展戰略,也是醫療科技發展的必然方向。2022年全國兩會期間,諸多人大代表圍繞干細胞產業發展紛紛建言。
結語:這些都意味著細胞治療時代,已經悄然來到我們身邊!在不久的將來,干細胞領域技術的不斷進步與發展將對人類疾病研究及壽命延長起到巨大作用。
版權聲明:本文資料來自網絡,目的在于介紹生物醫療領域前沿資訊、科學普及細胞領域的相關知識,僅用于分享、交流和學習,供訪問者參考。版權屬于原作者所有,如有侵權,請聯系我們及時刪除。




 掃碼添加官方微信
掃碼添加官方微信