糖尿病是困擾全球億萬患者的慢性代謝性疾病,長期以來,我們只能依靠胰島素和藥物來控制病情,但副作用和療效有限一直困擾著患者們。
利用干細(xì)胞治療數(shù)百萬糖尿病患者:方法、技術(shù)和未來方向
近期發(fā)表在權(quán)威期刊《Handbook of Stem Cell Applications》的一項研究,研究表明干細(xì)胞是一種可再生且安全的胰島來源,可實現(xiàn)廣泛的無免疫抑制胰島細(xì)胞移植,從而有望治愈糖尿病 (DM)。目前干細(xì)胞來源的胰島細(xì)胞移植臨床試驗的初步報告顯示出良好的前景。預(yù)計不久將有更多臨床試驗報告類似的有利結(jié)果,希望推動干細(xì)胞治療糖尿病的技術(shù)從考慮變?yōu)楝F(xiàn)實。

盡管優(yōu)化仍在進(jìn)行中,并且這些試驗的概念驗證在實施成為標(biāo)準(zhǔn)治療之前至關(guān)重要,但盡早考慮流程的可擴(kuò)展性以使數(shù)百萬糖尿病患者能夠獲得治療至關(guān)重要。規(guī)劃這些技術(shù)的成功意味著在引入干細(xì)胞來源的治療方法時盡早考慮方法、技術(shù)和工藝,以優(yōu)化當(dāng)前的研究并最大限度地發(fā)揮未來的效用。
在此,我們討論了干細(xì)胞來源的胰島細(xì)胞移植的兩個主要競爭者,即基于可誘導(dǎo)多能干細(xì)胞的自體胰島和同種異體胚胎干細(xì)胞來源的胰島,并評估了它們的可擴(kuò)展性潛力。此外,我們介紹了當(dāng)前對優(yōu)化細(xì)胞選擇和分化的人工智能方法的研究。我們還回顧了二維與三維培養(yǎng)技術(shù)和技術(shù)進(jìn)步,希望這些技術(shù)能夠在未來大規(guī)模生產(chǎn)干細(xì)胞衍生的胰島。
最后,我們討論了這些技術(shù)的一個重要現(xiàn)實考慮因素——全球4000萬糖尿病患者的成本和可及性。我們打算在研究早期強(qiáng)調(diào)可擴(kuò)展性問題的重要性,以解決此類問題并減少潛在的可擴(kuò)展性障礙,從而促進(jìn)數(shù)百萬患者早期廣泛獲得干細(xì)胞。
1型糖尿病:胰島免疫破壞與血糖穩(wěn)態(tài)失衡的雙重危機(jī)
1型糖尿病 (T1D) 涉及胰島的自身免疫性破壞,胰島負(fù)責(zé)胰腺的內(nèi)分泌功能。胰島由α細(xì)胞和β細(xì)胞組成,它們對局部環(huán)境作出反應(yīng),負(fù)責(zé)動態(tài)、反應(yīng)性血糖控制。
簡而言之,當(dāng)血糖過高(即高血糖癥)時,β細(xì)胞會釋放胰島素來降低血糖。當(dāng)血糖過低(低血糖癥)時,α細(xì)胞會釋放胰高血糖素來增加血糖。通過這種方式,胰島有助于身體穩(wěn)態(tài)并實現(xiàn)正常血糖(即葡萄糖水平從3.9到10mmol/L),無論葡萄糖攝入量如何,生理上都會迅速做出反應(yīng)。
因此,在患有T1D的患者中,如果沒有胰島來促進(jìn)血糖控制,則可能會發(fā)生高血糖和低血糖,導(dǎo)致兩種狀態(tài)下的嚴(yán)重后果。患有高血糖癥時,患者會出現(xiàn)排尿增多(即多尿)、口渴(即多飲)、惡心、嘔吐、腹痛、疲勞和口氣有水果味。從生理上講,當(dāng)身體不能適當(dāng)利用能量來源并轉(zhuǎn)變?yōu)榉纸獯x狀態(tài)以產(chǎn)生非葡萄糖源能量時,就會發(fā)生糖尿病酮癥酸中毒 (DKA)。由于脫水、酸中毒和意識模糊加重,DKA會迅速成為一種危及生命的疾病,死亡率為0.3–1.3%。
長期來看,高血糖會導(dǎo)致嚴(yán)重的微血管和大血管并發(fā)癥,包括冠狀動脈疾病、外周血管疾病、神經(jīng)病變、腎病和視網(wǎng)膜病變,從而大大降低生活質(zhì)量和時間。
另一方面,低血糖會立即導(dǎo)致自主神經(jīng)和神經(jīng)性低血糖并發(fā)癥,包括顫抖、嗜睡、視力和言語問題、心悸、焦慮,以及最令人擔(dān)憂的意識喪失(即糖尿病昏迷)和死亡。長期來看,低血糖會導(dǎo)致患者失去對這些事件的意識(即低血糖無意識),并給1型糖尿病患者帶來相當(dāng)大的發(fā)病率和死亡率風(fēng)險。
1922 年之前,1型糖尿病的死亡率極高,患者通常在出現(xiàn)癥狀后數(shù)周內(nèi)就會死亡,而且沒有可用的治療方法。1922年1月,在動物模型上取得成功后,加拿大多倫多的班廷博士、貝斯特和麥克勞德使用分離胰島素治療了第一位1型糖尿病患者,患者在持續(xù)治療下存活了13年,這在當(dāng)時是一項了不起的成就。班廷和麥克勞德獲得了1923年諾貝爾醫(yī)學(xué)獎。盡管有這一了不起的發(fā)現(xiàn),但班廷明白胰島素只是一種治療方法,而不是治愈方法,他在獲獎感言中指出:
胰島素不是糖尿病的治愈方法,而是一種治療方法。它使糖尿病患者能夠燃燒足夠的碳水化合物,從而可以在飲食中添加足夠數(shù)量的蛋白質(zhì)和脂肪,為生活中的經(jīng)濟(jì)負(fù)擔(dān)提供能量。
過去一百年來,我們對胰島素的應(yīng)用驗證了這一觀點。盡管胰島素的發(fā)現(xiàn)使患者得以避免高血糖和低血糖的急性并發(fā)癥,但外源性胰島素的血糖控制仍不完善。
胰島素治療的局限性:盡管胰島素挽救了T1D患者的生命,但外源性胰島素?zé)o法完全模擬胰島細(xì)胞的動態(tài)血糖調(diào)節(jié)功能,導(dǎo)致慢性并發(fā)癥(如血管病變)和低血糖風(fēng)險持續(xù)存在。
血糖控制現(xiàn)狀:目前,成年患者達(dá)標(biāo)率低,僅21%的美國成年 T1D 患者 HbA1c<7%(目標(biāo)值)。此外,兒童改善有限;青少年患者平均 HbA1c 仍高達(dá) 9.0%,與 1980 年代相比無顯著進(jìn)步。
低血糖風(fēng)險:31-41% 患者經(jīng)歷過低血糖,夜間發(fā)生率高且危害大(如意識喪失、癲癇)。
技術(shù)進(jìn)展的不足:現(xiàn)有胰島素泵、閉環(huán)系統(tǒng)等技術(shù)未能完全解決血糖波動問題,需進(jìn)一步優(yōu)化。
未來方向:開發(fā)更接近生理性調(diào)節(jié)的 β 細(xì)胞替代療法(如干細(xì)胞分化技術(shù)),以徹底改善 T1D 患者的血糖控制和生活質(zhì)量。
2型糖尿病的代謝困境與胰島移植的應(yīng)用挑戰(zhàn)
糖尿病(DM)的臨床負(fù)擔(dān)不僅限于1型患者,全球超過4億的2型糖尿病(T2D)患者面臨高血糖和低血糖的雙重風(fēng)險,其病理機(jī)制涉及胰島素分泌不足、胰島素抵抗及代償功能缺陷。盡管患者胰島未完全喪失,但仍會出現(xiàn)與1型糖尿病相似的代謝紊亂及并發(fā)癥。當(dāng)前治療以口服藥物為主,通過促進(jìn)殘存胰島功能或改善胰島素敏感性控制血糖;約15%患者因病情進(jìn)展需依賴胰島素。胰島移植(ITx)理論上可提供生理性血糖調(diào)節(jié),但因終身免疫抑制風(fēng)險及供體稀缺,目前極少用于T2D患者。然而,技術(shù)優(yōu)化或可突破免疫抑制限制,未來或惠及遠(yuǎn)超1型患者數(shù)量的龐大群體,但需解決可擴(kuò)展性問題。
為恢復(fù)生理性血糖調(diào)控,胰腺移植與ITx均被探索,但各有局限。胰腺移植雖能完全恢復(fù)內(nèi)分泌功能,但手術(shù)風(fēng)險高且依賴免疫抑制;ITx雖微創(chuàng)且圍手術(shù)期風(fēng)險低,卻受限于供體質(zhì)量不足、免疫排斥及免疫抑制副作用。兩者均因供體短缺難以滿足數(shù)億患者需求,故需嚴(yán)格分配標(biāo)準(zhǔn),目前ITx僅適用于伴嚴(yán)重低血糖或血糖極度不穩(wěn)定的1型患者。未來技術(shù)革新或能突破供體與免疫抑制瓶頸,但需平衡療效與可行性。
干細(xì)胞衍生胰島移植——突破糖尿病治療的供體與免疫抑制瓶頸
干細(xì)胞衍生胰島移植(SC-ITx)為克服傳統(tǒng)胰島移植(ITx)的供體短缺與免疫抑制依賴提供了革命性路徑。通過誘導(dǎo)性多能干細(xì)胞(iPSC)等分化技術(shù),可大規(guī)模生產(chǎn)功能性胰島,臨床試驗已初步驗證其安全性與療效。相較于依賴逝者供體的同種異體移植,SC-ITx的無免疫抑制潛力(如自體或免疫保護(hù)型移植)有望惠及更廣泛患者群體,包括4億2型糖尿病患者(T2D),同時避免自身免疫復(fù)發(fā)風(fēng)險。其目標(biāo)不僅是治愈約400萬1型糖尿病(T1D)患者,更可能重塑糖尿病整體治療格局。
實現(xiàn)這一愿景需在研發(fā)早期融入可擴(kuò)展性設(shè)計。需權(quán)衡同種異體與自體SC-ITx的規(guī)模化潛力,結(jié)合人工智能優(yōu)化細(xì)胞篩選,并深入解析干細(xì)胞擴(kuò)增條件以生產(chǎn)高效、功能性胰島(圖1)。此外,跨學(xué)科協(xié)作與自動化生產(chǎn)系統(tǒng)的整合將提升效率與經(jīng)濟(jì)性,確保技術(shù)從實驗室到臨床的快速轉(zhuǎn)化。通過系統(tǒng)性突破技術(shù)瓶頸,SC-ITx或能真正成為覆蓋億萬糖尿病患者的普適性療法,終結(jié)傳統(tǒng)治療的局限性。
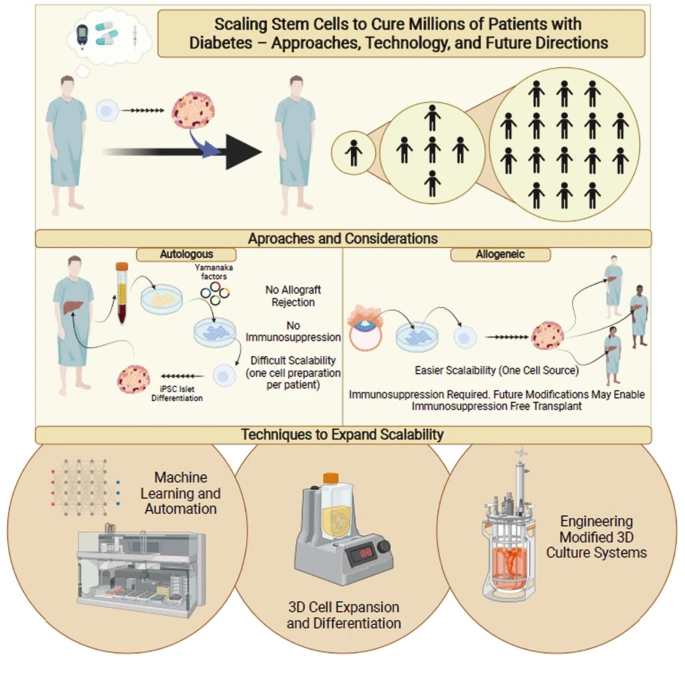
同種異體干細(xì)胞與自體干細(xì)胞的比較
目前正在研究兩種SC衍生ITx方法。每種方法都有其優(yōu)點、缺點和可擴(kuò)展性的獨特考慮因素。在本章的這一部分中,我們將討論這兩種方法的可擴(kuò)展性考慮因素。同種異體SC衍生ITx涉及少量SC供體作為分化和胰島生成的來源。雖然由于 SC 來源較少,可能更容易擴(kuò)展以進(jìn)行廣泛應(yīng)用,但對免疫抑制或免疫保護(hù)的要求可能會限制其整體風(fēng)險收益狀況。
或者,自體iPSC衍生的ITx涉及生成患者特定的iPSC以生成胰島,從而無需任何免疫抑制要求;但是,由于這種方法需要個體化的iPSC和胰島,因此優(yōu)化可擴(kuò)展性的技術(shù)對于實現(xiàn)廣泛使用至關(guān)重要。
同種異體干細(xì)胞胰島移植的優(yōu)勢與臨床突破
同種異體SC衍生ITx涉及多個胚胎或誘導(dǎo)多能 SC 作為所有接受者生成胰島的來源。這些 SC 來源在體外擴(kuò)增,分化為胰島,并作為同種異體 ITx 提供給患者。該技術(shù)可以將 SC 擴(kuò)增為大型生物反應(yīng)器,以產(chǎn)生數(shù)百萬個細(xì)胞進(jìn)行分化。同樣,從這種擴(kuò)增的 SC 來源分化可以更容易地產(chǎn)生幾個分化的胰島用于 ITx。雖然這種方法的可擴(kuò)展性可以消除 ITx 的胰島來源限制,但如果不進(jìn)一步修改流程,由于胰島來??源為同種異體,患者仍然需要免疫抑制。
同種異體干細(xì)胞胰島移植優(yōu)勢
供體供應(yīng)無限制:通過胚胎干細(xì)胞(ESC)或誘導(dǎo)多能干細(xì)胞(iPSC)體外擴(kuò)增分化,可規(guī)模化生產(chǎn)數(shù)百萬胰島細(xì)胞,突破傳統(tǒng)胰島移植的供體短缺瓶頸(Saima & Haider, 2021)。
技術(shù)可行性高:利用生物反應(yīng)器實現(xiàn)干細(xì)胞擴(kuò)增與定向分化,工藝可標(biāo)準(zhǔn)化,便于大規(guī)模應(yīng)用。
初步臨床驗證成功:Vertex公司VX-880胚胎干細(xì)胞胰島移植聯(lián)合免疫抑制治療,使1型糖尿病(T1D)患者胰島素依賴顯著減少,血糖控制改善;
ViaCyte公司干細(xì)胞胰島樣產(chǎn)品在皮下裝置中成功分泌C肽(Shapiro et al., 2021)。
免疫調(diào)控潛力:基因編輯技術(shù)(如敲除HLA-I類分子、表達(dá)IL-10或PD-L1)可降低免疫原性,減少或避免免疫抑制需求。
同種異體干細(xì)胞胰島移植成果與進(jìn)展
- 基因工程胰島:通過改造干細(xì)胞表達(dá)免疫耐受分子或消除HLA抗原,降低T細(xì)胞、巨噬細(xì)胞及NK細(xì)胞攻擊風(fēng)險;
- 封裝技術(shù):免疫保護(hù)裝置(如ViaCyte VC-02)在臨床試驗中初步顯示安全性與C肽分泌能力(NCT03162926),但需解決長期異物反應(yīng)問題。
- 肝外移植嘗試:皮下、網(wǎng)膜等部位移植雖在動物模型中有效,但臨床轉(zhuǎn)化仍面臨功能維持與免疫保護(hù)挑戰(zhàn)。
結(jié)論:同種異體干細(xì)胞胰島移植已展現(xiàn)突破供體限制與改善療效的潛力,但需進(jìn)一步解決免疫抑制、功能穩(wěn)定性及規(guī)模化生產(chǎn)難題,以實現(xiàn)從“概念驗證”到“普惠療法”的跨越。
自體干細(xì)胞胰島移植的優(yōu)勢與成果
第二種干細(xì)胞衍生胰島移植(SC-ITx)的替代方法涉及個體化生成誘導(dǎo)多能干細(xì)胞(iPSCs),并將其分化為胰島后進(jìn)行自體移植。該技術(shù)首先需從患者體細(xì)胞生成iPSCs:通過過表達(dá)山中因子(Oct3/4、Sox2、Klf4和c-Myc)將體細(xì)胞重編程為多能干細(xì)胞。
自體干細(xì)胞胰島移植的優(yōu)勢
- 完全免疫豁免:自體iPSC來源的胰島與患者遺傳背景一致,移植后無需免疫抑制,避免藥物副作用及感染風(fēng)險。
- 高度個性化:基于患者自身細(xì)胞重編程,無倫理爭議,且規(guī)避同種異體移植的免疫排斥問題。
- 技術(shù)可遷移性:分化方案與移植技術(shù)已通過同種異體SC-ITx臨床驗證(如Vertex公司案例),可直接轉(zhuǎn)化至自體治療場景。
自體干細(xì)胞胰島移植的成果與進(jìn)展
- 臨床前驗證成功:iPSCs分化胰島在動物模型中成功逆轉(zhuǎn)糖尿病;使用PBMC與仙臺病毒轉(zhuǎn)導(dǎo)技術(shù),已實現(xiàn)符合GMP標(biāo)準(zhǔn)的iPSCs生產(chǎn)。
- 分化流程成熟:iPSC向胰島的分化路徑已明確,可生成功能性β細(xì)胞。
結(jié)論:自體iPSC衍生胰島移植憑借免疫豁免與個性化優(yōu)勢,為糖尿病治愈提供理想路徑,但需突破規(guī)模化生產(chǎn)與成本限制,通過AI與自動化技術(shù)推動其從實驗室走向臨床普惠。
人工智能在優(yōu)化細(xì)胞選擇與分化中的作用
如上所述,自體干細(xì)胞衍生胰島移植(SC-ITx)的第一步是生成患者特異性的誘導(dǎo)多能干細(xì)胞(iPSC)系。為實現(xiàn)這一目標(biāo),需采集患者體細(xì)胞(通常為外周血單核細(xì)胞PBMC)并進(jìn)行體外擴(kuò)增。隨后,利用仙臺病毒轉(zhuǎn)導(dǎo)技術(shù),使細(xì)胞表達(dá)山中因子(Oct3/4、Sox2、Klf4和c-Myc),從而重編程為iPSCs。仙臺病毒轉(zhuǎn)導(dǎo)能高效遞送基因且不整合至宿主基因組。然而,僅1%-3%的PBMC能成功轉(zhuǎn)化為iPSCs,且需傳代約10次以清除病毒殘留。此后,需根據(jù)形態(tài)學(xué)手動篩選最佳iPSC克隆,并通過流式細(xì)胞術(shù)、基因分析、病毒篩查等技術(shù)進(jìn)行多維度表征,最終選定無遺傳異常且多能性標(biāo)記表達(dá)最優(yōu)的克隆。從iPSC生成到分化為胰島的全程耗時約2個月,涉及每日精細(xì)操作。
目前,iPSC的生成和分化都是手動完成的。然而,特定的形態(tài)和生長動力學(xué)細(xì)胞特征使得能夠自動選擇最佳的 PBMC 來生成 iPSC。同樣,可以使用自動化技術(shù)選擇最佳的iPSC克隆。我們的實驗室已經(jīng)展示了使用人工智能 (AI) 技術(shù)識別、追蹤和選擇最佳iPSC克隆的能力(圖2)。
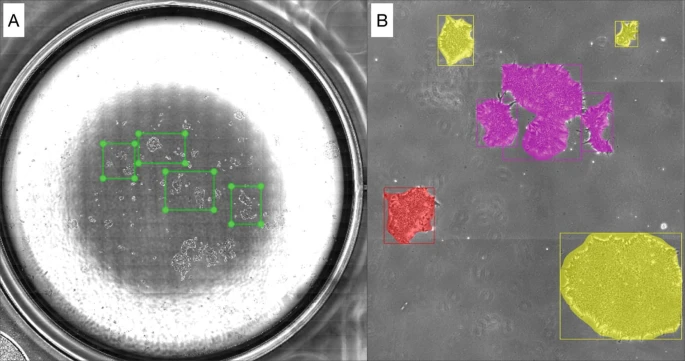
(a)自動選擇 iPSC 菌落以跟蹤生長和擴(kuò)增。(b)人工智能根據(jù)細(xì)胞形態(tài)、生長和擴(kuò)增率選擇最佳 iPSC 克隆以供選擇。
當(dāng)前流程高度依賴人工,但人工智能(AI)技術(shù)正推動其自動化與精準(zhǔn)化。例如:
AI優(yōu)化克隆篩選:通過機(jī)器學(xué)習(xí)識別iPSCs的形態(tài)與生長特征,自動選擇最優(yōu)克隆。
自動化擴(kuò)增與分化:如Cellino Biotech結(jié)合無標(biāo)記成像與AI算法,在封閉系統(tǒng)中篩選并擴(kuò)增iPSCs;Stem Cell Factory機(jī)器人系統(tǒng)實現(xiàn)從復(fù)蘇、培養(yǎng)到分化的全流程自動化。
質(zhì)量與效率提升:自動化系統(tǒng)生產(chǎn)的細(xì)胞均一性更高、分化能力更強(qiáng),且成本顯著降低。
AI技術(shù)同樣適用于同種異體SC-ITx的胚胎干細(xì)胞(ESC)擴(kuò)增與維護(hù),通過標(biāo)準(zhǔn)化流程提升細(xì)胞系穩(wěn)定性并降低人工成本。從而提高同種異體SC衍生的ITx的潛力。
患者可及性和費用
幸運的是,對AI方法、自動化技術(shù)、3D 培養(yǎng)條件和技術(shù)進(jìn)步的經(jīng)濟(jì)評估已經(jīng)顯示出可觀的預(yù)期節(jié)省。經(jīng)濟(jì)分析表明,盡管前期成本較高,但在生成和維護(hù) iPSC 系時,與手動技術(shù)相比,自動化系統(tǒng)在機(jī)器預(yù)期的 8 年使用壽命內(nèi)總體可節(jié)省 42%(圖3)。
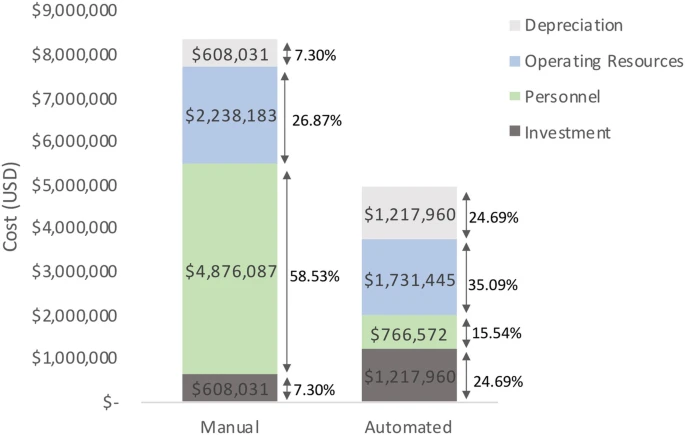
同樣,與2D培養(yǎng)條件相比,3D培養(yǎng)條件下的細(xì)胞擴(kuò)增已被證明可將擴(kuò)增能力提高至少十倍,從而進(jìn)一步降低成本。通過優(yōu)化3D細(xì)胞培養(yǎng)和擴(kuò)增實現(xiàn)的潛在90%的節(jié)省以及自動化系統(tǒng)實現(xiàn)的42%的節(jié)省,我們認(rèn)為可以實現(xiàn)一種具有成本效益的SC衍生ITx方法。這與CAR-T細(xì)胞療法的成本降低類似,CAR-T細(xì)胞療法最初每位患者細(xì)胞治療的費用超過一百萬美元,但現(xiàn)在已降至每位患者不到10萬美元,而且許多大學(xué)都具備成本效益高的生產(chǎn)能力。
我們猜測SC衍生的ITx也存在類似的趨勢,希望能夠為數(shù)百萬患者提供廣泛的應(yīng)用。考慮到目前糖尿病治療及其并發(fā)癥的費用是大多數(shù)國家的主要醫(yī)療支出,潛在的節(jié)省是巨大的。
過結(jié)合人工智能、自動化和優(yōu)化的3D培養(yǎng)系統(tǒng),在不久的將來,生成用于移植的SC衍生胰島的成本可能會大幅下降。臨床前研究已經(jīng)引起了包括ViaCyte Inc.和Vertex Pharmaceuticals在內(nèi)的企業(yè)合作伙伴的興趣,以實施臨床試驗。如果臨床試驗繼續(xù)顯示出令人鼓舞的結(jié)果,那么這筆投資可能會增長,并有能力支付自動化和大型商業(yè)生物反應(yīng)器的前期成本。
盡管SC衍生ITx具有可獲得、成本合適的潛力,但研究人員和資助者在與私營部門合作時應(yīng)該了解這些療法的投資潛力,并考慮患者的可獲得性。正如本文所討論的那樣,數(shù)百萬患者將從這些療法中受益;為所有這些患者提供經(jīng)濟(jì)上可獲得的治療方法是觸手可及的,并且仍然掌握在目前正在研究和實施這些方法的研究人員手中。
結(jié)論
隨著細(xì)胞療法不斷優(yōu)化,有望治愈糖尿病,我們必須考慮我們面臨的疾病范圍。超過四百萬患者患有1型糖尿病,超過四億患者患有糖尿病。開發(fā)一種僅對部分患者無法獲得或無法擴(kuò)展的療法或潛在治愈方法不應(yīng)被視為一種選擇。
在整個研究、開發(fā)和臨床試驗過程中,我們必須繼續(xù)研究和優(yōu)化能夠?qū)崿F(xiàn)可擴(kuò)展方法的技術(shù)。與工藝開發(fā)一樣,促進(jìn)技術(shù)和自動化擴(kuò)展的早期優(yōu)化和協(xié)作應(yīng)繼續(xù)成為優(yōu)先事項。如果我們繼續(xù)考慮這些技術(shù),那么生產(chǎn)一種可獲得且經(jīng)濟(jì)高效的細(xì)胞產(chǎn)品可以治愈數(shù)百萬患者。
參考資料:Verhoeff, K., Shapiro, A.M.J. (2024). Scaling Stem Cells to Cure Millions of Patients with Diabetes: Approaches, Technology, and Future Directions. In: Haider, K.H. (eds) Handbook of Stem Cell Applications. Springer, Singapore. https://doi.org/10.1007/978-981-99-7119-0_18
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。




 掃碼添加官方微信
掃碼添加官方微信