干細胞治療被譽為繼藥物和手術之后的新醫學革命,在治療神經系統疾病、心血管病、骨關節損傷等方面展現出巨大潛力。然而,對于這種神奇的細胞,它們是如何進入我們體內、能否“聰明”地找到病灶,以及不同的注射方式有何區別,公眾仍存在許多疑問。本文將通過解答七個關鍵問題,為您揭開干細胞治療的神秘面紗。

疑問一:干細胞通過何種方式進入人體?
干細胞并非憑空出現在病灶,其進入人體依賴于精密的醫療遞送技術,主要分為三大途徑:
全身性播散——靜脈輸注:如同點滴輸液,將干細胞懸液通過外周靜脈注入血液循環。
- 首過效應(First Pass Effect):首次通過肺部毛細血管床時,大量干細胞(尤其是直徑較大的細胞)會發生機械性滯留,隨后緩慢釋放。這意味著只有一小部分細胞能進入全身血液循環并到達非肺部損傷點。
- 適用性:廣泛應用于系統性炎癥、心臟病(如心肌梗死后)、糖尿病等全身或彌散性疾病。
中樞直通車——鞘內注射:通過腰椎穿刺,將干細胞直接注射到包裹著大腦和脊髓的腦脊液中。
- 目的:規避血腦屏障 (BBB),使干細胞能通過腦脊液的循環,直接到達大腦、腦干和脊髓表面的損傷區域。
- 適用性:脊髓損傷、肌萎縮側索硬化癥(ALS)、腦癱、多發性硬化癥等中樞神經系統疾病。
精準靶向投放——局部注射:在影像技術引導下,將干細胞精準注射至病灶區域,如心肌梗死區、損傷的關節腔內或視網膜下。
- 優勢:最大化了細胞在目標部位的濃度,顯著減少了全身分布和免疫排斥的風險。
- 適用性:骨關節炎、局部缺血性肢體病、肌肉損傷、傷口修復等。
疑問二:注入后,干細胞能自己“找到”損傷位置嗎?
答案是:能,但效率有限。這一過程被稱為“歸巢”。
這是一個關于干細胞“歸巢”(Homing)的關鍵問題,干細胞具有一定的趨向性,但并非百分之百的“精準導彈”(圖1)[1]。

間充質干細胞的系統性歸巢包括五個不同的步驟,包括黏附和滾動、激活、細胞停滯、滲出或跨內皮遷移以及遷移。
干細胞,尤其是間充質干細胞(MSC),具有天然的歸巢特性。當身體組織發生損傷、炎癥或缺血時,受損部位會釋放出特定的信號分子,如:
- 趨化因子(Chemokines)
- 細胞因子(Cytokines)
- 生長因子(Growth Factors)
這些信號分子就像“導航燈”,能夠被干細胞表面的相應受體識別。干細胞會沿著這些信號的濃度梯度移動,穿過血管壁,到達損傷區域并聚集。
然而,現實并非完美。靜脈注射的干細胞如同被投入急流的救援隊,大量細胞會被肺、肝、脾等器官“截留”,最終僅有約1%-5%能成功歸巢到靶點。因此,提高歸巢效率是當前研究的關鍵突破點。
疑問三:歸巢效率如此低,治療還有效嗎?
這引出了干細胞發揮作用的另一核心機制——旁分泌效應[2]。
研究發現,干細胞修復組織的關鍵,未必在于大量分化為新細胞直接“補缺”。更重要的是,它們如同“微型藥廠”,在歸巢途中和到達后,能持續分泌大量生物活性因子:
- 營養與修復因子:如VEGF、BDNF,促進血管新生、保護受損細胞、刺激內源性修復。
- 免疫調節因子:調節炎癥環境,從“破壞性炎癥”轉為“修復性炎癥”。
- 細胞外囊泡(外泌體):攜帶蛋白質、核酸等信息物質,調控周圍細胞行為。
因此,即使少數干細胞抵達,也能通過強大的旁分泌作用,改善損傷部位的“土壤”(微環境),喚醒機體自身的修復潛能。這正是干細胞治療有效的底層邏輯之一。
疑問四:大腦有堅固的“血腦屏障”,干細胞如何進入并修復神經?
血腦屏障(BBB)是一道由腦血管內皮細胞和緊密連接構成的嚴密防線,它可以阻止血液中的有害物質進入大腦,但也極大地限制了干細胞通過靜脈輸注進入中樞神經系統(CNS)。
針對大腦和CNS疾病的治療,主要采取以下策略:
- 局部繞行:采用鞘內注射或腦室注射。這繞過了血管系統,將干細胞直接遞送到腦脊液中。通過腦脊液的循環,干細胞可以更直接、更高效地接觸到脊髓和大腦的受損區域。
- 短時開放:研究人員正在探索通過某些藥物或超聲技術[3],暫時、可逆地打開血腦屏障,以便靜脈注射的干細胞能夠進入大腦(圖3)。
- 跨屏障機制:少數干細胞可能通過特殊的跨細胞轉運或在炎癥狀態下通透性增加的血管進入大腦。
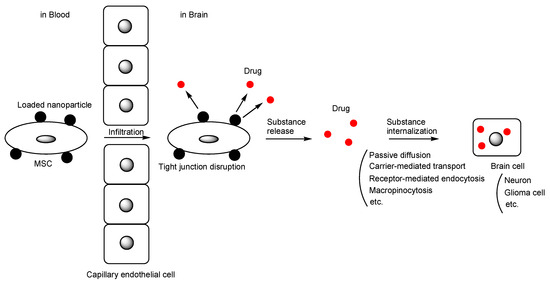
除了鞘內/腦室注射這種直接繞行的策略外,研究還探索了其他潛在機制:
- 炎癥/損傷誘導滲透性增加:在嚴重損傷(如腦卒中、創傷性腦損傷)急性期,BBB的通透性會暫時增加,為靜脈輸注的干細胞提供了一個短暫的進入“窗口”。
- 鼻腔遞送:鼻腔粘膜下的神經末梢可作為干細胞進入CNS的潛在通道,該方法具有非侵入性的優勢,但到達效率尚待優化。
- 外泌體遞送:由于外泌體體積微小(30-150nm),它們更容易穿透BBB,將干細胞的修復信號(如miRNA和蛋白質)遞送到腦部損傷灶。
疑問五:不同的注射方式,對療效有決定性影響嗎?
是的,注射方式是療效的“戰略決策”。它直接決定了干細胞的初始分布、存活率和作用模式(表1)。
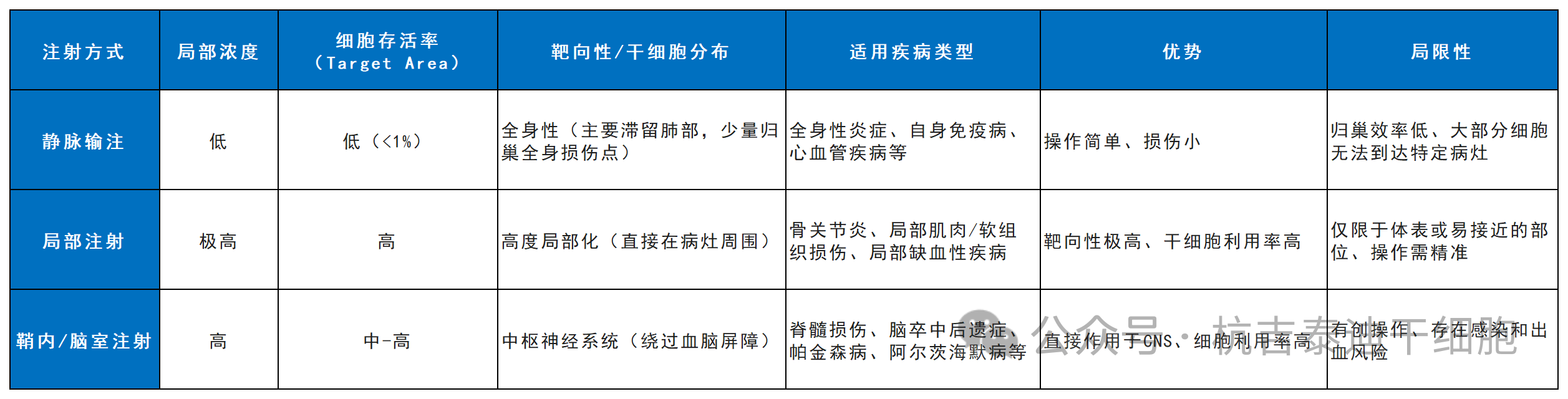
疑問六:干細胞到達后,究竟如何“修復”損傷?
修復是一個多管齊下的協同過程:
- 細胞替代與融合:在適宜條件下,少量干細胞可分化為神經元、星形膠質細胞等,直接替換死亡細胞;或與現有細胞融合,提供支持。
- 營養與保護:分泌的神經營養因子,宛如“強心針”,滋養瀕死神經元,延長其存活時間。
- 調控微環境:調節免疫反應,減輕有害炎癥;促進血管新生,為受損區域恢復血液供應。
- 激活內源干細胞:喚醒大腦中處于休眠狀態的神經干細胞,促進其增殖分化,實現自我更新。
疑問七:干細胞治療的未來趨勢是什么?
為了提高干細胞治療的效果和安全性,未來的研究重點主要集中在以下方面:
- 增強歸巢能力:通過基因工程或體外預處理技術,改造干細胞使其表面受體表達更高,從而更有效地識別和到達損傷部位。
- 優化細胞載體:使用生物材料支架或水凝膠等,將干細胞包裹后遞送,提高細胞在病灶處的存活率和作用時間。
- 細胞無細胞療法:集中研究干細胞分泌的外泌體(Exosomes)等旁分泌產物。這些“干細胞信使”具有低免疫原性、易儲存和易穿透屏障的優勢,有望成為更安全的治療新方向。
總結而言,干細胞治療是一個從“精準遞送”到“智能修復”的復雜系統工程。 它不僅是細胞的簡單移植,更是對機體修復機制的深度動員與重啟。
盡管歸巢效率、屏障跨越等挑戰依然存在,但隨著遞送技術、生物工程和材料科學的進步,我們正朝著讓干細胞治療變得更精準、更高效、更安全的目標穩步邁進。每一次科學的突破,都在為無數患者點亮再生與康復的希望之光。
參考資料:
[1]:Umar Sajjad, Muhammad Ahmed, M Zohaib Iqbal, Mahrukh Riaz, Muhammad Mustafa, Thomas Biedermann, Agnes S Klar, Exploring mesenchymal stem cells homing mechanisms and improvement strategies, Stem Cells Translational Medicine, Volume 13, Issue 12, December 2024, Pages 1161–1177, https://doi.org/10.1093/stcltm/szae045
[2]:Gnecchi, M., Danieli, P., Malpasso, G., Ciuffreda, M.C. (2016). Paracrine Mechanisms of Mesenchymal Stem Cells in Tissue Repair. In: Gnecchi, M. (eds) Mesenchymal Stem Cells. Methods in Molecular Biology, vol 1416. Humana Press, New York, NY. https://doi.org/10.1007/978-1-4939-3584-0_7
[3]:Tashima, T. Mesenchymal Stem Cell (MSC)-Based Drug Delivery into the Brain across the Blood–Brain Barrier. Pharmaceutics 2024, 16, 289. https://doi.org/10.3390/pharmaceutics16020289
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信