二十多年來,基于人類多能干細胞 (hPSC) 的帕金森病 (PD) 療法研究已在臨床試驗中取得階段性成果。首份關于患者自體hPSC移植的臨床報告顯示,患者的運動癥狀顯著改善,證實了該方法的治療前景。
然而,關鍵挑戰依然存在,尤其是供體細胞的植入和存活率有限。hPSC在體外分化為中腦多巴胺能祖細胞和神經元的過程中產生的細胞應激,導致移植的mDA神經元存活率降低。此外,由于注射損傷、免疫排斥以及PD患者腦內存在的α-突觸核蛋白病理,注射部位的宿主腦環境對移植細胞變得不利。
多能干細胞治療帕金森病上市難在哪?攻克細胞存活與免疫排斥成關鍵!
基于目前多能干細胞治療帕金森病存在一系列問題,2025年6月底,國際期刊雜志《延世醫學雜志》發表了一項“基于人類多能干細胞的帕金森病療法:挑戰與潛在解決方案”的研究綜述。

綜述著重探討了應對內在供體細胞應激和不利宿主腦環境的潛在策略,旨在提高基于hPSC的PD細胞療法的長期療效和植入率。
帕金森病的病理特征與機制
帕金森病(PD)作為第二大神經退行性疾病,核心病理表現為中腦黑質(A9區)多巴胺能神經元的進行性退化,導致運動功能障礙。
其關鍵病理驅動因素是α-突觸核蛋白(α-syn)的異常聚集:生理狀態下,α-syn參與突觸傳遞和基因調控,但錯誤折疊后形成的聚集體可引發線粒體損傷、內質網應激、自噬-溶酶體功能障礙及突觸/核異常,形成惡性循環加速神經元死亡。此外,細胞外釋放的α-syn聚集體通過激活神經膠質炎癥反應加劇神經炎癥,并以朊病毒樣方式經突觸傳播至鄰近神經元,推動病變擴散。

現有治療局限與替代療法探索
當前PD治療依賴多巴胺能藥物和深部腦刺激(DBS)緩解癥狀,但無法阻斷疾病進展。針對病理機制的疾病修飾療法(如靶向α-syn聚集體、神經炎癥通路)正通過抗體、小分子、外泌體及基因療法積極研發。
理想的治療策略是細胞替代療法——移植健康多巴胺神經元至中腦。早期胎兒中腦組織移植雖在部分患者中實現>10年的癥狀改善,但因移植細胞數量和功能不可控,導致療效不一致且可能引發運動障礙等副作用,雙盲試驗未能證實其持續有效性。
干細胞療法的潛力
干細胞技術為細胞替代療法提供新方向:具備自我更新和分化為中腦多巴胺(mDA)神經元能力的干細胞,可替代倫理受限的胎兒組織。其優勢在于實現標準化、可控的DA神經元植入,規避倫理爭議,并提供穩定供體來源,有望成為PD細胞治療的關鍵突破點。
以干細胞為基礎的干細胞替代療法治療帕金森病的研究歷史
中腦干細胞療法的核心挑戰:開發基于干細胞(胎兒腹側中腦干細胞)的帕金森病 (PD) 療法的重點在于確保干細胞具備中腦多巴胺(mDA)神經元的生成潛能。
干細胞雖具有自我更新和多向分化能力,但這些特性隨其發育階段而異:mDA神經元形成于腹側中腦(VM)早期發育階段,源自該階段的干細胞能高效生成mDA神經元。然而,當通過擴增獲取足量細胞時,此類干細胞易喪失原有mDA神經發生能力。這些腦組織源性干細胞的局限性制約了其在PD細胞療法中的應用。
胚胎干細胞的突破性進展:小鼠胚胎干細胞(mESCs)因無限增殖和全能性優勢,成為替代組織干細胞的理想選擇。關鍵突破始于Lee團隊首次成功誘導mESCs分化為mDA神經元,后續研究證實移植此類細胞可恢復PD大鼠運動功能。這一成果推動了多能干細胞(PSCs)作為PD治療來源的廣泛探索。
人源干細胞的轉化困境:在驗證了mESC衍生細胞后,下一步是轉向人類PSC(hPSC),例如人類ESC(hESC)和人類誘導PSC(hiPSC),以開發用于帕金森病患者的潛在供體細胞(表1)。
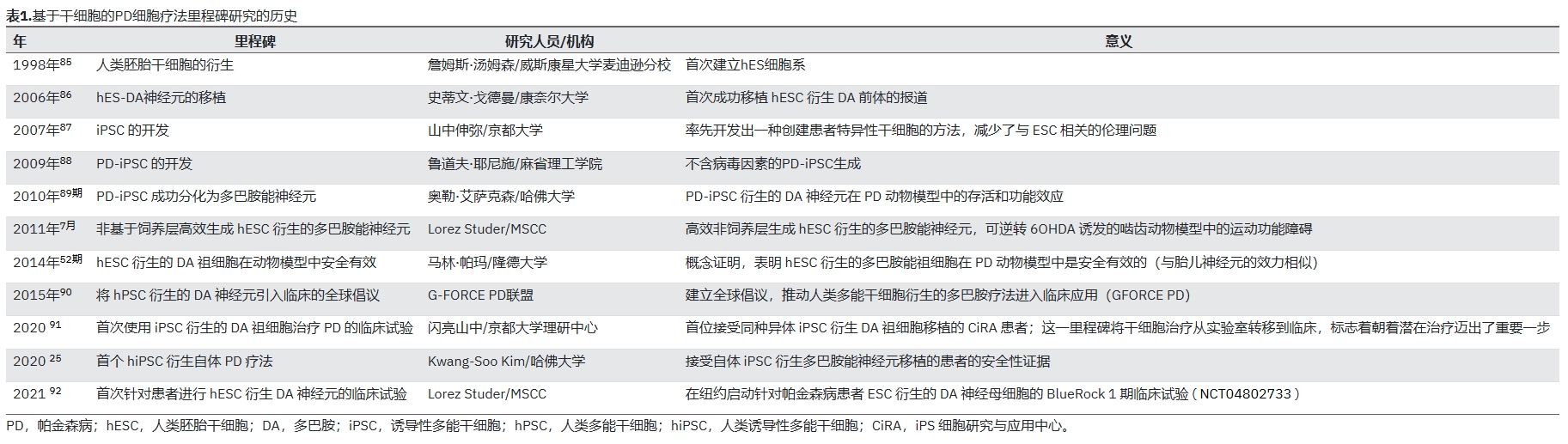
早期分化嘗試效率低下:傳統方法(如擬胚體形成或基質細胞共培養)產生的DA神經元常缺失中腦特異性標記物(如Nurr1、Foxa2、Lmx1a、En-1)。這些標記物對神經元存活、抗毒性損傷及突觸形成至關重要,是療效實現的必要條件。
發育路徑模擬的臨床轉化:基于mDA神經元源自底板區的發育特性,斯隆-凱特琳研究所的Studer團隊創新性模擬該路徑,使hESCs分化出表達全套中腦標記物的mDA神經元。其方案(經改良或原版)至今廣泛沿用,并在人源化小鼠及非人靈長類PD模型中證實:移植hPSC衍生的mDA祖細胞可實現神經整合與運動功能恢復,為臨床轉化奠定基礎。
最近,這項研究的臨床試驗結果已經出爐:重磅!帕金森病再生療法突破:hESC衍生多巴胺能神經元在I期試驗展現安全性與功能恢復潛力。
基于人類多能干細胞治療帕金森病的臨床轉化最新進展
隨著基于hPSC的帕金森病(PD)療法研究的進展,全球范圍內針對PD患者的臨床試驗正在啟動和籌備中(表2)。第一份基于hPSC的帕金森病細胞療法臨床報告由哈佛大學發表,詳細介紹了一項利用患者來源的hPSC進行自體移植的PD患者治療方案。
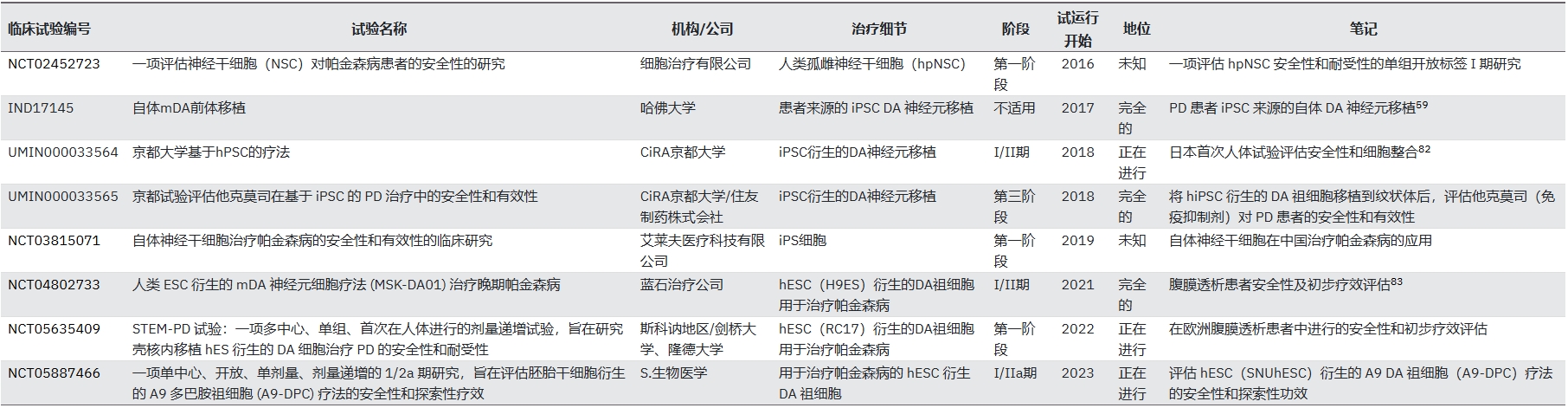
臨床評估表明,移植后18至24個月,帕金森病癥狀趨于穩定或改善,證明了干細胞治療的安全性和初期療效。然而,帕金森病癥狀的持續改善仍值得懷疑。這一結果強調,有必要改進細胞療法,以確保更有效、更持久地緩解癥狀,且不產生不良反應。
干細胞療法助力治療帕金森病:2025年1-5月全球研究突破與臨床轉化新趨勢
供體細胞存活和植入是干細胞治療帕金森病的關鍵挑戰
要使hPSC衍生的mDA祖細胞發揮治療作用,供體細胞必須存活,分化為成熟的mDA神經元,并與宿主腦神經元形成突觸連接。在這些過程中,供體細胞存活率低是最大的挑戰。而存活的供體細胞的mDA神經元分化/成熟以及與宿主神經元的突觸整合相對有效。臨床試驗中,移植后患者大腦的PET成像始終顯示mDA神經元植入水平明顯低于預期。
限制供體細胞存活和植入的因素
移植操作的急性損傷機制(針傷問題):哈佛大學最新研究揭示,超過90%的移植多巴胺(DA)神經元在植入早期死亡,一周內達峰值。其核心機制是注射針頭造成的機械損傷觸發宿主腦內小膠質細胞及外周T細胞浸潤,釋放TNF-α、IFN-γ等促炎因子,直接誘導DA神經元急性死亡。進一步研究發現,TNF-α通過激活p53通路介導神經元退化,構成移植后細胞快速損失的關鍵分子路徑(圖1)。
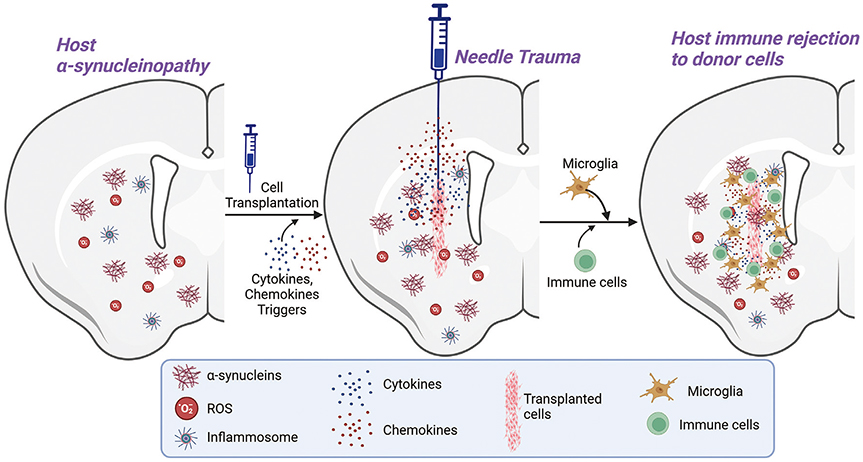
在帕金森病細胞移植中,細胞被注射到已經出現嚴重 α-突觸核蛋白病、活性氧 (ROS) 和炎癥的病理性腦環境中。移植針的使用會進一步誘發創傷,觸發先天免疫反應因子的釋放,例如促炎細胞因子和趨化因子。這些因素會激活周圍的神經膠質細胞,并促進外周免疫細胞向腦內浸潤,從而可能加劇炎癥反應并阻礙組織修復。總而言之,這些機制對移植細胞的存活和整合產生了不利影響。
宿主病理環境的慢性威脅(α-突觸核蛋白擴散):帕金森病腦中錯誤折疊的α-突觸核蛋白(α-syn)不僅具有直接神經毒性,還能以朊病毒樣方式跨神經元傳播。尸檢研究證實,移植入患者腦內的胎兒中腦組織同樣出現α-syn病理擴散。這提示宿主病理環境會持續威脅供體細胞——但當前主流臨床前模型(6-OHDA嚙齒類與MPTP靈長類)均缺乏α-syn病理特征,導致移植細胞在真實患者腦中面臨三重未被充分評估的威脅:毒性α-syn積累、病理增殖及神經炎癥微環境(圖1)。
關于帕金森病細胞移植中宿主免疫排斥問題
免疫排斥的雙重挑戰與機制:移植的DA神經元的持久性受到宿主不同程度免疫反應的顯著影響。這些移植細胞存活的關鍵因素在于它們能否避免移植排斥,而這一過程受宿主的適應性免疫系統控制。
研究表明:自體誘導多能干細胞(iPSC)分化的DA神經元可顯著降低免疫反應,而同種異體移植則持續面臨排斥風險——即便在中樞神經系統(CNS)這一傳統”免疫豁免區”,血腦屏障(BBB)的完整性破壞(如帕金森病病理或手術創傷)仍會解除免疫保護。
人源化小鼠模型證實,人類白細胞抗原(HLA)不匹配的DA神經元移植會觸發免疫排斥,此外,大腦作為免疫豁免環境的地位似乎依賴于血腦屏障 (BBB) 的完整性。無論是帕金森病患者的大腦,還是外科手術干預,都可能損害血腦屏障(圖1)。
免疫抑制治療的矛盾性
手術針傷對BBB的破壞會啟動級聯炎癥:先天免疫系統被激活,釋放TNF-α、IL-1β、IFN-γ等促炎因子及趨化因子,引發小膠質細胞浸潤(Iba-1+標志)和MHC-II+抗原呈遞細胞聚集。為對抗排斥,免疫抑制治療成為必要手段,但長期使用他克莫司、硫唑嘌呤等藥物與實體器官移植患者的癌癥風險上升相關。盡管干細胞治療帕金森病的免疫抑制劑副作用尚未大規模顯現,這一潛在安全風險仍需警惕(圖1)。
供體細胞在體外制備過程中積累的細胞應激問題
體外制備過程中的多重應激累積:hPSC分化為治療性mDA神經元的關鍵步驟——腹側中腦(VM)模式化,面臨雙重應激源:高密度培養所需的細胞間物理擠壓,以及模式化誘導因子的化學毒性。這些體外制備壓力在分化早期即開始累積,形成移植前固有的細胞損傷基礎,直接威脅后續移植存活率。
中腦保護因子的環境敏感性困境:當前分化方案雖能賦予細胞中腦特異性保護因子(如抗毒性損傷蛋白),但這些因子在宿主腦的氧化/炎癥環境中極易失活。研究證實其敏感性源于宿主移植位點的應激微環境。因此,未來技術突破需聚焦于:開發即使在惡劣環境下也能穩定表達中腦特異性因子的mDA神經元的制備方案,仍然是增強供體細胞適應力的重要目標(圖1)。
優化多能干細胞治療帕金森病的潛在解決方案
優化多能干細胞治療帕金森病方案之一供體細胞制備
改進mDA神經元分化方案
2D培養體系的固有缺陷:現有hPSC分化方案在二維(2D)高密度培養中進行腹側中腦(VM)模式化,雖為神經誘導所必需,但雙重壓力源導致細胞應激累積:
- 物理壓力:極高細胞密度引發接觸性擠壓
- 化學毒性:模式化因子(如SMAD抑制劑)直接損傷細胞
后果:分化細胞提前積累衰老、線粒體功能障礙等應激損傷,降低移植存活率。
3D類器官技術的突破性優勢:通過三維(3D)類器官培養模擬體內微環境,實現革命性改進。
- 類器官衍生神經干細胞(Og-NSC):從第18天VM類器官分離,顯著降低細胞衰老/線粒體應激水平,保持強勁增殖能力與mDA分化潛能,支持大規模生產。
- 高效分化驗證:Og-NSC分化的mDA神經元持續高表達關鍵標記物(Foxa2、Nurr1、En-1),在PD大鼠模型中證實運動功能恢復效果提升。
- 技術普適性:點狀”3D模式化技術同樣實現高效分化,驗證3D路徑普適價值
未來協同強化方向:為應對宿主腦內惡劣環境,需多策略協同。
- 靶向關鍵應激通路:明確p53是宿主環境中激活的核心損傷信號(阻斷可提升抗逆性);
- 跨平臺技術整合:結合基因編輯(增強保護基因表達)、抗氧化劑預處理等;
- 抗炎-抗氧化聯合設計:開發兼具炎癥抵抗與氧化應激耐受的”超級供體細胞”。
技術意義:3D培養不僅解決細胞制備應激問題,更為構建適應宿主病理的韌性細胞奠定基礎,推動PD細胞治療向臨床轉化邁出關鍵一步。
優化多能干細胞治療帕金森病方案之一優化人多能干細胞產業標準化建立
hPSC的革命性潛力與細胞系篩選:人源多能干細胞(hPSC,含hESC與hiPSC)憑借無限擴增和分化為功能性細胞的能力,為帕金森病細胞療法提供變革性平臺。臨床前研究證實:ESC衍生的多巴胺能祖細胞療效可媲美胎兒中腦移植。成功的關鍵在于優選具有定向分化傾向的細胞系——如RC17、H9及SNUhES1-ESC系能穩定分化為A9型多巴胺神經元(帕金森病治療靶點),目前已在臨床試驗中驗證(表2)。
hiPSC的免疫優勢與潛在風險:hiPSC技術通過重編程體細胞實現個體化治療,其核心價值在于潛在避免免疫排斥:自體細胞可被識別為”自身”,理論上無需免疫抑制。但爭議點在于:
- 免疫原性不確定性:重編程過程可能引發異常免疫反應
- 疾病病理攜帶風險:患者來源的hiPSC可能繼承α-突觸核蛋白病理傾向
- 規模化瓶頸:個體化制備面臨高昂成本與生產周期挑戰
安全性和標準化生產的技術突破:為確保臨床安全,hPSC建立需三重保障:
- 基因組穩定性:采用非整合重編程技術(如游離載體)避免插入突變;
- 殘留細胞清除:通過流式分選/抗體介導剔除未分化多能細胞(防畸胎瘤);
- 通用型解決方案:開發HLA配型庫或基因編輯”通用供體”hiPSC系降低免疫風險。
全鏈條質控推動臨床轉化:從實驗室到臨床的轉化依賴標準化體系:
- 多維度質控:涵蓋多能性標記物驗證(OCT4/NANOG)、核型分析及體內外分化效能測試
- 工藝可擴展性:建立自動化培養系統實現批次一致性生產
- 監管合規性:遵循GMP規范制備臨床級細胞產品
該框架不僅適用于帕金森病,更為神經退行性疾病的干細胞治療提供范式。
優化多能干細胞治療帕金森病方案之一緩解惡劣的宿主大腦環境
調節性T細胞(Treg)的聯合移植
針對移植針傷引發的急性神經炎癥導致中腦多巴胺(mDA)神經元大量死亡的問題,哈佛團隊創新性地將外周血來源的Treg細胞與hPSC衍生的mDA祖細胞共移植。
該策略基于Treg在腦損傷修復中的關鍵作用——通過抑制促炎因子釋放(如TNF-α、IFN-γ)和減少免疫細胞(小膠質細胞/T淋巴細胞)浸潤,有效阻斷針傷后的炎癥級聯反應。在帕金森病嚙齒類模型中,共移植使mDA神經元存活率顯著提升,并增強運動功能恢復,為克服細胞治療早期移植損耗提供了轉化潛力。
星形膠質細胞聯合移植
星形膠質細胞是大腦中最豐富的神經膠質細胞,發揮著重要的神經營養和穩態功能。它們通過清除活性氧等機制保護神經元免受細胞內外毒性的侵害,清除過量的興奮毒性谷氨酸,并去除有害脂質。此外,星形膠質細胞還會釋放神經營養因子和抗炎細胞因子,進一步支持神經元健康。
我們最近的研究強調了星形膠質細胞(特別是源自VM的星形膠質細胞)在緩解α-syn病理方面的治療潛力。這些VM星形膠質細胞通過多種機制發揮作用:
- 1) 通過旁分泌信號抑制神經元α-突觸核蛋白的聚集和傳遞;
- 2) 釋放分解細胞外α-突觸核蛋白聚集體的因子;
- 3) 主動清除細胞外α-突觸核蛋白原纖維;
- 4) 通過旁分泌作用刺激神經元自噬清除α-突觸核蛋白。
鑒于α-突觸核蛋白病理的傳遞是維持長期治療益處的重大挑戰,利用這些保護性功能使星形膠質細胞移植成為治療神經退行性疾病的一種有前景的方法。
針對宿主免疫細胞的策略
急性免疫反應的致命性挑戰:移植后一周內,針傷引發的宿主免疫應答迅速啟動:CD4/CD8 T淋巴細胞與小膠質細胞、星形膠質細胞大量浸潤移植區,釋放TNF-α、IFN-γ等促炎因子,直接導致90%以上移植mDA神經元急性死亡。這一過程凸顯抑制早期細胞因子風暴(尤其TNF-α/p53通路)是提升供體細胞存活的關鍵靶點(圖1)。
腦內駐留免疫細胞具有雙面性:在正常生理條件下,小膠質細胞和星形膠質細胞發揮神經營養和神經支持作用。然而,針刺損傷會使它們極化為促炎狀態。鑒于這種膠質細胞極化是可逆的,因此促進其從促炎表型轉變為神經營養表型的策略很有前景。此外,通過募集宿主Treg細胞至移植部位來調節炎癥T細胞活性,可以進一步減少免疫介導的損傷并提高移植物的存活率。
免疫抑制策略的現狀與優化方向:自體移植細胞可能因表達新抗原觸發免疫反應,而同種異體mDA神經元必然面臨宿主排斥風險——需建立約150個HLA匹配的iPSC庫實現人群覆蓋,但當前同種異體療法仍依賴免疫抑制劑防止移植物衰竭。
臨床實踐采用多藥聯用方案:Transneuro試驗單用他克莫司;NYSTEM試驗組合他克莫司+霉酚酸酯+巴利昔單抗+潑尼松龍;STEM-PD試驗包含硫唑嘌呤四聯方案。鑒于長期免疫抑制的致癌/感染風險,亟需通過個體化給藥(依據HLA錯配度調整劑量/療程)、時序化干預(急性期強化后遞減)及新型緩釋技術優化治療窗,平衡移植物存活與患者長期安全。
從生存瓶頸到功能重塑——干細胞治療帕金森病的破局之路
干細胞療法已實現從實驗室到臨床的跨越:2025年全球多項試驗證實,hPSC分化的多巴胺神經元可穩定整合于患者腦內,部分患者運動評分改善達40%(UPDRS-III)。然而>90%移植細胞在植入一周內死亡的生存瓶頸,成為制約療效的核心障礙。其本質是三重絞殺——針傷引發的TNF-α/p53死亡風暴、宿主α-突觸核蛋白的朊病毒樣擴散、以及HLA錯配導致的免疫排斥——共同構成細胞存活的“不可能三角”。
破局性新策略:免疫-細胞協同調控正開辟新路徑:
- 細胞韌性革新:3D類器官衍生的Og-NSC使線粒體應激降低60%,關鍵中腦因子(Foxa2/Nurr1)表達穩定性提升3倍;
- 免疫微環境重塑:Treg聯合移植通過抑制小膠質細胞浸潤,將動物模型存活率提升250%;
- 病理防御升級:腹側中腦星形膠質細胞移植可清除α-突觸核蛋白原纖維(清除率>80%),阻斷宿主病理擴散。
這些策略使“功能性治愈”存活閾值從<10%突破至>30%。
未來進化方向:終極目標是從“存活”邁向“功能重建”:
- 精準遞送:磁共振引導聚焦超聲(MRgFUS)實現非侵入式血腦屏障開放,減少針傷90%;
- 動態監控:單細胞測序技術實時追蹤移植細胞命運,指導個體化免疫抑制方案;
- 通用型治療:CRISPR構建的HLA隱身iPSC庫(全球需150系)進入Ⅲ期臨床(中國NCT2025-0810)。當干細胞突破三重絞殺,帕金森病的神經修復將迎來真正的生物學治愈時代。
終極愿景:當干細胞從“存活”邁向“功能整合”,當免疫調控從“抑制排斥”升級為“主動耐受”,帕金森病的治愈曙光將不再遙不可及——這場對抗神經退行的戰役,終將以人類對細胞命運的精準駕馭而改寫結局。
主要參考資料:
[1]Chang MY, Lee SH. Human Pluripotent Stem Cell-Based Therapies for Parkinson’s Disease: Challenges and Potential Solutions. Yonsei Med J. 2025 Jul;66(7):395-404. https://doi.org/10.3349/ymj.2024.0447
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信